化妆品与皮肤科学 | 《化妆品生产质量管理规范检查要点及判定原则》实施后广州市化妆品生产许可现场核查常见问题分析

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效

引用本文



何羡霞,胡树文,陈晓丽,姜志辉*.《化妆品生产质量管理规范检查要点及判定原则》实施后广州市化妆品生产许可现场核查常见问题分析[J].中国食品药品监管.2026.02(265):143-149.
《化妆品生产质量管理规范检查要点及判定原则》实施后广州市化妆品生产许可现场核查常见问题分析
Analysis of Common Issues in On-site Licensing Inspections of Cosmetic Manufacturers in Guangzhou Following Implementation of the Inspection Key Points and Determination Principles for Cosmetic Good Manufacturing Practices
何羡霞
广州市食品药品审评中心
HE Xian-xia
Guangzhou Center for Food and Drug Evaluation
胡树文
广州市食品药品审评中心
HU Shu-wen
Guangzhou Center for Food and Drug Evaluation
陈晓丽
广州市食品药品审评中心
CHEN Xiao-li
Guangzhou Center for Food and Drug Evaluation
姜志辉∗
中国人民解放军南部战区总医院药学部
JIANG Zhi-hui∗
Department of Pharmacy, General Hospital of Southern Theater Command of PLA
摘 要Abstract
目的:评估《化妆品生产质量管理规范检查要点及判定原则》(以下简称《检查要点》)实施后广州市化妆品生产许可现场核查的情况,分析企业在适应新规过程中的主要挑战,为提升行业质量管理水平提供科学依据。 方法:基于2023 年广州市617 家化妆品生产企业的现场检查数据,采用描述性统计与归因分析法,重点研究缺陷项目的分布特征、高频违规条款的表现形式及其成因。 结果:《检查要点》实施后,广州市化妆品生产许可核查不通过率达46. 35%,主要问题集中在质量保证与控制、厂房设施与设备管理、物料与产品管理、生产过程管理四个方面。 结论:广州市化妆品生产企业在新规实施初期面临较大合规压力,现场检查中暴露出质量体系运行不规范、生产条件与管理水平不足等突出问题。企业需加强质量管理体系建设和硬件投入,监管部门则应优化分级分类监管机制、强化行业引导和信息公开。
Objective:This study evaluates the status of on-site licensing inspections for cosmetic manufacturers in Guangzhou following the implementation of the Inspection Key Points and Determination Principles for Cosmetic Good Manufacturing Practices hereinafter referred to as the Inspection Key Points . It further analyzes the main challenges faced by manufacturers in complying with the new requirements and provides evidence-based recommendations for improving quality management in the cosmetic industry. Methods:On-site inspection data from 617 cosmetic manufacturers in Guangzhou in 2023 were analyzed using descriptive statistics and root cause analysis.The study focused on the distribution of deficiency items the occurrence patterns of high-frequency non-compliance clauses and their underlying causes. Results:The failure rate of licensing inspections reached 46. 35% after the new regulations took effect. Most deficiencies were concentrated in four areas quality assurance and control facility and equipment management material and product management and production process management. Conclusion:In the initial stage of the new regulation cosmetic manufacturers in Guangzhou faced substantial compliance pressure. On-site inspections revealed systemic weaknesses including inconsistent quality management system operations substandard production conditions and inadequate management practices. To address these issues manufacturers should strengthen their quality management systems and invest in infrastructure improvements while regulatory authorities should optimize tiered and categorized supervision mechanisms provide stronger industry guidance and enhance information transparency.
关键词Key words
化妆品生产;质量管理;现场检查;检查要点;缺陷分析
cosmetic manufacturing;quality management system;on-site inspection;inspection key points;deficiency analysis
基金项目



广州市校(院)企联合资助项目(2024A03J0644)

化妆品行业作为时尚与健康产业的重要组成部分,其产品质量直接关系到消费者的健康与安全[1,2] 。中国作为全球化妆品消费大国[3-5] ,近年来不断加强对化妆品行业的监管力度,以提升产品质量, 保障消费者权益。为规范化妆品生产许可和监督检查工作,国家药品监督管理局( 以下简称国家药监局) 依据《化妆品监督管理条例》[6] 及《化妆品生产经营监督管理办法》[7] 等法规、规章,组织制定并发布了《化妆品生产质量管理规范》[8,9] 及其配套文件《化妆品生产质量管理规范检查要点及判定原则》[10] ( 以下简称《检查要点》)。《检查要点》自2022 年12 月1 日起施行,它不仅对化妆品生产过程中的质量管理提出了更加具体和严格的要求,也对化妆品生产企业的现场检查工作带来了新的挑战。
广州市作为中国化妆品产业的重要基地之一,拥有众多化妆品生产企业。据《2023 广州化妆品产业白皮书》显示[11] ,截至2023 年9 月,广州市共有化妆品生产许可证持证企业1870 家, 占广东省(3152 家) 的59.3%,占全国( 5561 家) 的33.6%;广州市化妆品产值达1000 亿元,占全省总量的70%以上,居全国首位。《检查要点》的落地实施,对广州市化妆品企业的生产流程、质量监控体系及监管合规性提出了更高的要求,同时也为提升化妆品生产质量管理水平和现场检查效率提供了新的契机。
在此背景下,本文以《检查要点》实施后的广州市化妆品生产许可现场核查为研究对象,基于2023 年1 月~12 月的核查数据,统计分析企业在执行规范过程中存在的共性问题,旨在评估当前化妆品生产质量管理水平,并提出相应的改进建议,为推动化妆品生产行业的高质量发展提供参考。
1 广州市化妆品生产许可现场核查总体情况
2023 年1 月~12 月,广州市食品药品审评中心共派出专职检查员1234 人次,依据《检查要点》(实际生产版) 对617 家化妆品生产企业进行生产许可现场核查。在全部617 家企业的检查中,现场核查结论为不通过的286 家次,整改后复查的331 家次。具体情况见表1。

2 现场核查不通过企业缺陷项目分布情况
表1 统计数据显示,2023 年广州市化妆品生产企业现场核查不通过率高达46.35%,反映出行业在《检查要点》实施初期面临较大的合规压力。对不通过企业的缺陷项目分布进行分类发现,质量保证与控制( 21.48%)、物料与产品管理(21.41%)、生产过程管理( 21.24%) 及厂房设施与设备管理(19.47%) 四大板块构成了主要问题领域,合计占比高达83.6%。具体情况见表2。
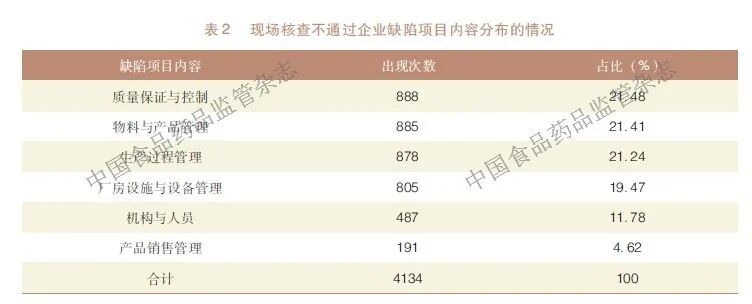
对现场核查不通过企业的缺陷项目条款进行统计(见图1),出现频次排名前十的缺陷项目条款依次为25*、47*、16*、6*、62*、32*、23*、50*、68*、74**。除条款6*是质量安全负责人履职相关的条款,其他高频条款均对应主要问题四大板块。下文将针对该四大板块,分析高频问题的具体表现及成因。
3 检查现场高频问题的具体表现与分析
3.1 质量保证与控制
如表2 所示, 质量保证与控制相关条款缺陷共计888 次,占比21.48%。《检查要点》中该部分共设置16 条检查条款,其中5 条属于重点项目(*), 11 条属于一般项目。如图1 所示, 在现场核查不通过的企业中,质量保证与控制方面的高频条款依次为25*、16*、23*,其检查要点主要涉及以下三方面内容:企业是否配备与生产的化妆品品种、数量和生产许可项目等相适应的检测能力,包括设施设备和检验人员;制定的原料、内包材、半成品以及成品的内控标准是否符合强制性国家标准和技术规范,且按内控标准检验放行;建立的记录管理制度是否明确了记录的填写、保存、处置等程序和格式,并按制度执行。
现场检查过程中发现的典型问题包括:①企业配备的检验设施设备、仪器试剂等条件不足,如企业申请生产润肤油( GB/T 29990-2013)、按摩精油(GB/T 26516-2011) 等产品,但未具备该类产品出厂检验中过氧化值、酸值等项目的检测条件;②企业配备的检验员能力不足,如在现场考核过程中,检验员对所申请生产的洗发水有效成分检测或微生物检测等项目不熟悉;③记录管理混乱,部分企业提供的批生产记录存在随意更改或未如实记录实际生产情况的问题。
质量保证与控制是企业质量管理体系的核心构成,企业应高度重视该领域的建设,增加对检测设施设备、仪器试剂的投入,确保检验条件与生产需求相匹配。其次,应加强对检验人员的专业培训,提高其对产品检验标准和操作流程的熟悉度,同时落实对关键岗位人员的考核管理。此外,还应建立健全内部监督机制,确保各项质量管理制度得到严格执行。
3.2 物料与产品管理
如表2 所示,物料与产品管理相关条款缺陷共计885 次,占比21.41%。根据《检查要点》,该部分共设14 条检查条款,其中关键项目1 条(49**),规定企业不得使用禁用原料、未经注册或者备案的新原料,不得超出使用范围、限制条件使用限用原料,并确保原料、外购的半成品、内包材符合法律法规、强制性国家标准及技术规范的要求;7 条为重点项目(*), 主要涉及供应商管理、物料审查、进货查验、工艺用水、产品合规、标签管理等方面;此外还有6 条属于一般项目。如图1所示,在现场核查不通过的企业中,物料与产品管理方面的高频条款主要为47*、50*,检查要点聚焦供应商管理和物料进货查验两方面的内容。
在现场检查过程中,企业问题主要表现为:①未建立合格物料供应商名录或建立的供应商名录信息不全,如未记录已使用合格物料的生产企业信息,或记录的供应商信息与提供的采购合同中的供应商信息不一致;②企业未明确关键原料供应商,或未明确关键原料供应商需要进行现场审核的情形,或明确了却未按规定执行;③企业一般侧重于来料检验,但未在制度上明确物料验收标准和验收方法,亦未按要求留存需进口原料及国内物料的合格出厂证明文件、送货票证、报关单等相关证明;④部分企业提供的出厂检验报告(Certificate of Analysis,COA) 与原料仓库实际的物料标签标示的批号、数量、生产日期不一致,未达到确保物料质量的要求。
物料与产品管理覆盖了从供应商管理、物料审查、物料验收、物料贮存到物料放行的全流程,确保化妆品从原料到成品的每个环节都符合质量要求,是化妆品生产全过程管理的重要一环,也是保证化妆品质量安全的关键因素。但从现场检查情况看,企业对物料及产品管理的能力及力度仍有待加强,建议企业加强物料管理,严格执行进货查验制度,从源头上筑牢质量安全屏障。
3.3 生产过程管理
如表2 所示,生产过程管理方面相关条款缺陷共计878 次,占比21.24%。根据《检查要点》,该部分共设16 条检查条款,其中关键项目2 条(61**、74**),重点项目2 条(62*、68*),其余12 条为一般项目。关键项目关注企业是否按照化妆品注册、备案资料载明的技术要求建立并执行产品生产工艺规程和岗位操作规程, 是否按照化妆品注册、备案资料载明的技术要求生产产品(61**),以及企业是否确保产品经检验合格且检验项目至少包括出厂检验项目, 是否确保相关生产和质量活动记录经质量安全负责人审核批准(74**)。重点项目则聚焦企业的主要生产工艺是否经过验证,是否保存验证方案、记录及报告(62*),以及企业是否遵循生产工艺规程和岗位操作规程,生产记录是否可以如实反映整个生产过程(68*)。如图1 所示,在现场核查不通过的企业中,生产过程管理方面的高频缺陷条款主要集中在62*、68*、74**。
在现场检查过程中,企业问题主要表现为:①未制定工艺验证管理规程,无法提供生产产品的工艺验证方案和报告,或提供的工艺验证报告无具体的原始数据记录; ②企业提供的批生产记录未如实反映整个生产过程的情况,如提供的领料记录与配制记录中的物料不一致,或配制记录的出料量与灌装的领料量不一致,亦或由成品计算出来的料体数量与配制工序的出料量不一致;③企业已销售产品的成品检验记录显示出厂项目检验不全,或者产品未经质量负责人放行审核批准即上市销售。
生产过程管理是化妆品质量保障体系中的核心环节,在《检查要点》中涉及该方面的条款占据了2 条关键项目,是一票否决项。因此,企业应高度重视生产过程管理的制度建设与落实执行,严格工艺验证管理规程,规范生产记录,执行出厂检验与放行制度。
3.4 厂房设施与设备管理
如表2 所示,厂房设施与设备管理相关条款缺陷共计805 次,占比19.47%。《检查要点》中该部分共设置17 条检查条款,其中5 条属于重点项目(*),12 条属于一般项目。如图1 所示,在现场核查不通过的企业中, 厂房设施与设备管理方面的高频条款主要为32.,其检查要点包括:企业在生产施用于眼部皮肤表面以及儿童皮肤、口唇表面,以清洁、保护为目的的驻留类化妆品( 粉剂化妆品除外) 时,其半成品贮存、填充、灌装、清洁容器与器具贮存区域等是否符合生产车间洁净区的要求,如企业是否能提供年度洁净度报告,提供的洁净度报告中的生产车间平面图是否与实际平面图一致;日常环境监控的微生物指标是否符合《化妆品生产质量管理规范》附2 的要求;洁净区的静压差相对于一般生产区是否≥10Pa,相对于准洁净区是否≥5Pa。
现场检查过程中发现的典型问题包括: ①企业申请生产施用于眼部皮肤表面以及儿童皮肤、口唇表面,以清洁、保护为目的的驻留类化妆品( 粉剂化妆品除外),其半成品贮存、填充、灌装、清洁容器与器具贮存区域不符合生产车间洁净区的要求,其洁净区的静压差相对于一般生产区未≥ 10Pa,相对于准洁净区未≥5Pa;②企业提供的车间年度洁净度报告附上的生产车间平面图与实际检查看到的生产车间布局不一致,不符合《化妆品生产质量管理规范》附2 的要求;③部分企业在生产洁净区设置了一般清洗区,但未将一般清洗区进行物理隔离等。
厂房设施与设备是企业生产活动和产品质量保障的“硬实力”,企业应重视厂房设施设备的投入。高质量的厂房设施设备是生产高品质化妆品的基础,也是确保产品在生产过程中稳定性和安全性的重要保障,对企业的可持续发展具有关键作用。
4 讨论与建议
针对上述广州市化妆品生产企业在《检查要点》实施初期现场核查中暴露出的典型问题,本文从企业和监管部门两个维度提出以下对策与建议。
4.1 企业层面
对于企业而言,一是要切实加强质量体系建设[12] ,组织质量管理人员根据企业实际情况编制符合自身特点的质量管理体系手册,杜绝简单照搬其他企业的管理制度;同时应定期开展新体系文件的培训和宣贯,确保从管理层到关键岗位员工都能准确理解和掌握制度要求,做到知规、守规、履规。二是要进一步提高认识, 严格落实企业主体责任[13] 。注册人、备案人作为化妆品质量安全第一责任人,应强化风险意识,深刻理解化妆品生产过程中任何一个环节的疏漏都可能导致质量安全事故的发生。企业负责人应切实增强责任意识,深入学习相关法规和标准要求,始终牢记企业的主体责任,全面加强生产质量管理, 依法履行质量安全法律责任,确保产品质量安全万无一失。三是要加快推进厂房设施等硬件的升级改造[12] 。《化妆品生产质量管理规范》及《检查要点》对厂房设施与设备等硬件提出了更高的要求,企业应按照自身产品的工艺流程及环境控制要求升级改造生产车间,杜绝产能与设备不匹配的情况,要重点做好空气净化系统和水处理系统的日常维护与定期保养,确保关键生产设备始终处于良好运行状态,为产品质量的稳定可控提供坚实的硬件保障。
4.2 监管层面
对于监管部门而言,一是应进一步完善化妆品生产企业的分级分类监管机制,建立高风险企业监管名单,针对高风险企业,如近三年有抽检不合格产品的企业,应增加现场督查次数及抽检力度,提升监管精准性与靶向性。二是应鼓励化妆品相关行业协会在推动监管政策落地与企业引导方面发挥更积极的作用[14] 。监管部门可依托行业协会组织政策解读、技术研讨和合规培训,帮助企业提升法规意识、生产技术和质量管理水平,引导行业向规范化、标准化方向发展。三是加强信息公开,定期发布化妆品质量监管报告,对于遵守法规、质量管理水平高的企业,给予政策支持和奖励;对于存在违规行为的企业,依法依规从严处罚,形成有效的激励和惩戒机制。
第一作者简介
何羡霞,硕士,广州市食品药品审评中心,副主任药师。专业方向:药事管理、新药研发
通讯作者简介
姜志辉,博士,中国人民解放军南部战区总医院药学部,副主任药师。专业方向:药事管理、新药研发
参考文献:略




编辑:李丹
审核:赵燕宜


