第一三共/阿斯利康的「全球首发」给了中国

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效


3月27日,第一三共与阿斯利康宣布优赫得®(德曲妥珠单抗,T-DXd)序贯THP方案在中国获批,用于HER2阳性高危早期乳腺癌的新辅助治疗。随着该方案在全球首次获批,T-DXd正式从晚期后线治疗拓展至早期治愈的核心阵地。


优赫得®第7项适应症:早期乳腺癌的“降维打击”
此次附条件批准基于DESTINY-Breast11 III期研究,T-DXd序贯THP方案的病理完全缓解率达到67.3%,而当前HER2阳性早期乳腺癌的标准辅助治疗(ddAC-THP)为56.3%。
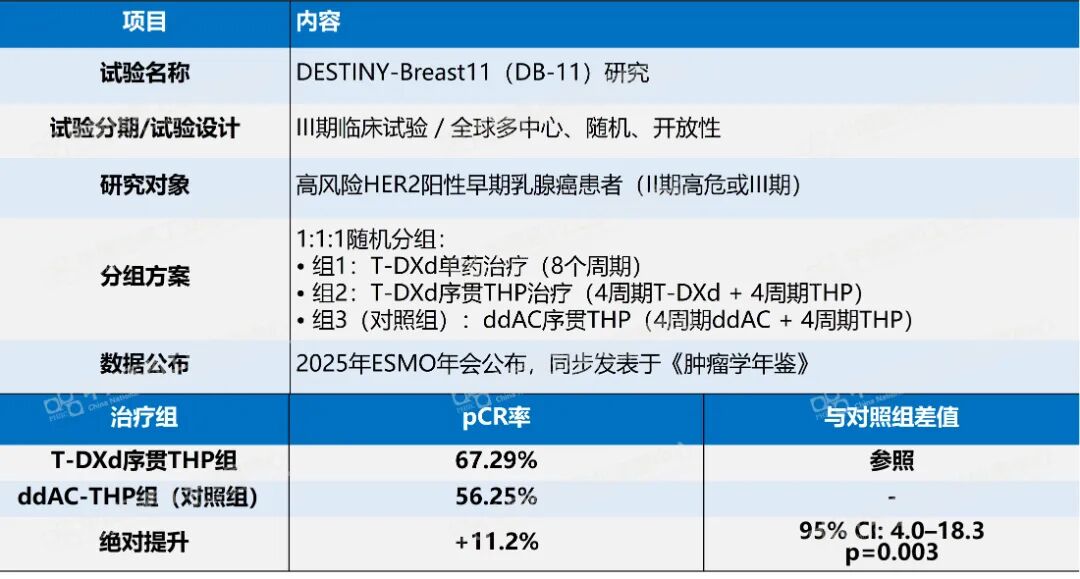
表1:DESTINY-Breast11 III期研究关键信息和主要终点
数据来源:Pharma ONE药物研发大数据平台-全球临床试验结果板块,中国医药工业信息中心
同时,安全性也有显著改善,T-DXd序贯THP方案成功规避了蒽环类药物长期困扰临床的心脏毒性风险。
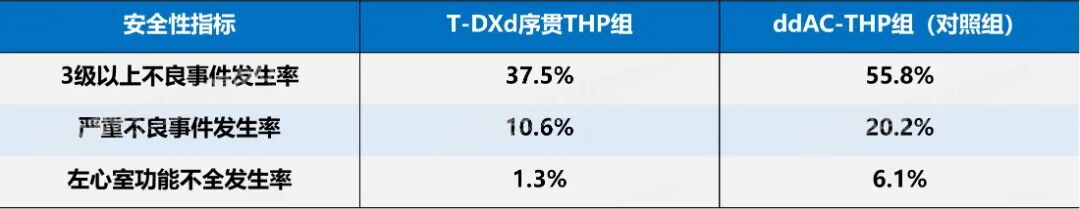
表2:DESTINY-Breast11 III期研究安全性数据
数据来源:Pharma ONE药物研发大数据平台-全球临床试验结果板块,中国医药工业信息中心
该项研究还设置了T-DXd单药治疗组,但由于独立数据监查委员会建议而提前终止入组,该组病理完全缓解率仅为43.0%,远低于联合治疗组。也就是说,在新辅助治疗阶段,T-DXd仍需与THP方案协同作战。这与T-DXd在晚期乳腺癌中“单药即王”的地位形成鲜明对比,早期治疗追求“根治”,需要多机制协同;晚期治疗主要为“控制”,ADC单药就能胜任。

ADC药物治疗:“度”的博弈与“位”的争夺
这项新适应症的获批,也将治疗决策引向一个核心命题:HER2阳性早期乳腺癌患者,到底应该做“减法”还是“加法”?
所谓“减法”,是对传统化疗方案进行精简,在保证疗效的前提下降低毒性。以卡铂的取舍为例,国内一项neoCARHP研究数据显示,在“曲妥珠单抗+帕妥珠单抗+紫杉类”的基础上去除卡铂后,pCR率仅从65.9%微降至64.1%,但3-4级不良事件发生率却从34.6%降至20.7%。可见疗效没掉,毒性显著降低。这类策略的目标人群是低中危患者,追求的是“疗效不减、毒性更优”。

信息来源:《Journal of Clinical Oncology》(JCO,影响因子43.4,中科院一区)
而DESTINY-Breast11 III期研究是做“加法”。研究入组的患者中近九成淋巴结阳性,45%以上为T3-4期局部晚期,是标准意义上的高危人群。这类患者需要更强的武器,T-DXd序贯THP方案将pCR率从56.3%提升至67.3%,为高风险人群提供了更优的术前控制方案。
两条路线是基于风险分层的一体两面,低中危患者考虑降阶梯治疗,高危患者考虑升级治疗。未来临床决策的关键是:对哪些人用ADC替代化疗,对哪些人用ADC序贯化疗。
放眼全球,HER2阳性乳腺癌的新辅助/辅助治疗标准,正随着新数据的出炉而悄然改写。2025年底公布的DESTINY-Breast05研究显示,在新辅助治疗后仍有残余病灶的患者中,T-DXd相比全球首个获批的 HER2 靶向ADC药物T-DM1(赫赛莱®,恩美曲妥珠单抗)可将复发风险降低53%,该结果撼动了T-DM1自2018年以来建立的“术后辅助金标准”地位。这项适应症在国内已拿下突破性疗法和上市申请受理,在美国获FDA优先审评,在欧盟也已获EMA受理审评。
国内的竞争格局同样精彩。就在本月,恒瑞医药登记了一项II期临床试验,直接头对头比较其自主研发的SHR-A1811(瑞康曲妥珠单抗)与T-DXd的疗效与安全性。恒瑞的策略很清晰:T-DXd在临床应用中最大的顾虑是间质性肺病(ILD),发生率约10%-12%,而SHR-A1811在早期研究中ILD发生率仅2.6%。恒瑞试图以“疗效可比+安全性更优”的组合拳,在ILD顾虑高的患者群体中争取份额。与此同时,科伦博泰的SKB264(芦康沙妥珠单抗)在HR阳性/HER2阴性乳腺癌中继续推进,百利天恒的BL-B01D1(EGFR/HER3双抗ADC)则选择“跨适应症错位竞争”,将主战场放在非小细胞肺癌和鼻咽癌。国产ADC们的集体策略是:不直接和T-DXd最强领域正面交锋,而是通过靶点差异化、适应症分层、安全性优化等路径寻找生存空间。

优赫得之外:第一三共的乳腺癌ADC家底
不止于单一产品,第一三共在乳腺癌ADC领域的打法,是一套“三层纵深”的体系。
第一层是HER2靶点的“饱和式覆盖”。T-DXd已从HER2阳性晚期二线、一线,覆盖至HER2低表达和超低表达,再到早期新辅助和辅助治疗。今年2月,该药用于新辅助治疗后non-pCR患者辅助治疗的适应症在欧盟获批;3月,FDA受理该适应症优先审评申请。T-DXd构建的从术前到术后的全病程闭环,是竞争对手目前无法复制的深度。
第二层是TROP2靶点的“第二增长曲线”。德达博妥单抗(Dato-DXd)今年2月获FDA优先审评,用于一线治疗不适合免疫治疗的三阴性乳腺癌。TROPION-Breast02研究显示,该方案可将中位总生存期延长5个月。在HR阳性/HER2阴性这一乳腺癌最大亚型中,Dato-DXd同样在推进布局,与德曲妥珠单抗形成互补。
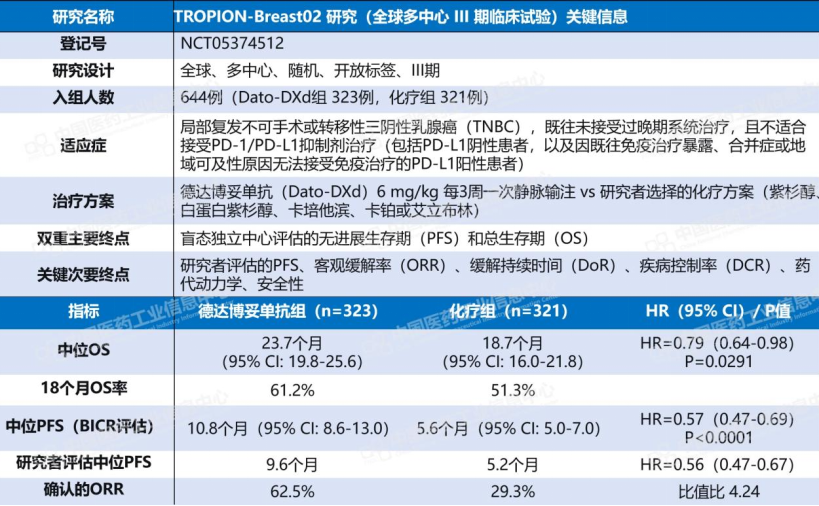
表3:TROPION-Breast02研究关键信息和主要指标
数据来源:Pharma ONE药物研发大数据平台-全球临床试验结果板块,中国医药工业信息中心
第三层是平台内部的“风险对冲”。根据Pharma ONE数据库显示,去年年底,靶向HER3的帕曲妥尤单抗(HER3-DXd)在III期研究中折戟,乳腺癌是该药物核心适应症之一,针对的是 HER3 表达的晚期/转移性乳腺癌后线治疗;加上今年DS-9606的研发被停止,使第一三共通过非乳腺癌领域的其他ADC管线(肺癌、卵巢癌)来分散风险、维持平台价值。
耐人寻味的是,T-DXd在中国的商业化表现远未达到市场预期。2025财年前三季度,其中国区销售额约0.95亿美元,仅占全球收入2.8%。医保谈判后23.7万元/年的治疗费用仍高于T-DM1的17.4万元,国产曲妥珠单抗生物类似药在下沉市场分流了大量患者,间质性肺病的顾虑也持续影响用药决策。今年3月,第一三共在中国启动的REFRESH真实世界研究中期分析显示,中国临床存在将T-DXd用于一线治疗的强烈需求,但也证实了本土化证据积累的必要性。
对于第一三共来说,挑战或许不是来自技术迭代的速度,而是如何找到全球化产品与本土化策略之间的平衡。
欢迎在评论区留下您的看法👏




