BMJ | 中国研究:卡瑞利珠单抗联合CAPOX方案改写晚期胃癌/食管胃结合部腺癌一线治疗格局

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效


3月12日,《英国医学杂志》(BMJ)在线发表了一项由沈琳教授领衔、全国75家中心参与的大型III期临床研究(NCT03813784)。该研究证实,在HER2阴性、不可切除的局部晚期或转移性胃/胃食管结合部腺癌一线治疗中,卡瑞利珠单抗联合CAPOX方案(卡培他滨+奥沙利铂)序贯卡瑞利珠单抗维持治疗,较单纯化疗显著延长总生存期。然而,在维持阶段加用抗血管生成药物阿帕替尼,不仅未能进一步延长生存,反而明显增加3级以上不良反应和治疗中止率。这一结果不仅为胃癌免疫治疗再添中国证据,也为临床实践中的维持治疗策略提供了重要警示:“加法”并非越多越好,精准选择才是关键。
研究背景
胃癌是全球第五大常见恶性肿瘤和第五大癌症相关死亡原因,尤其在亚洲地区发病率较高。由于早期症状不典型,多数患者确诊时已处于晚期,5年总生存率低于5%。约80%的胃癌患者为人表皮生长因子受体2(HER2)阴性,这类患者的治疗选择一直是临床研究的重点。
免疫检查点抑制剂的问世为HER2阴性胃癌的治疗带来了革命性变化。CheckMate 649、KEYNOTE-859等多项大型临床研究已证实,在标准化疗基础上加入PD-1抑制剂可显著改善患者生存,尤其对于PD-L1表达较高的患者。然而,在免疫联合化疗的方案中,化疗药物通常在使用4-6个周期后停用以减轻累积毒性,患者随后进入维持治疗阶段。目前,最佳的维持治疗策略尚未确定,免疫检查点抑制剂单药维持与联合用药的优劣比较缺乏前瞻性III期研究数据。
卡瑞利珠单抗是中国自主研发的PD-1抑制剂,阿帕替尼则是一种高度选择性的VEGFR-2酪氨酸激酶抑制剂,,已在中国获批用于晚期胃癌三线治疗。临床前研究提示,PD-1抑制剂与抗血管生成药物可能存在协同作用。基于此,研究者设计了这项三臂随机对照试验,旨在回答两个核心问题:免疫+化疗序贯免疫维持是否优于单纯化疗、在维持阶段加用阿帕替尼能否进一步增效?
研究设计与方法
这项多中心、随机、开放标签的3期试验在中国75家医院开展,旨在评估卡瑞利珠单抗联合CAPOX方案(卡培他滨+奥沙利铂)后接不同维持治疗方案对比单纯化疗在HER2阴性晚期胃癌或胃食管交界处腺癌一线治疗中的疗效和安全性。
研究纳入885例既往未经治疗、HER2阴性、不可切除的局部晚期或转移性胃癌或胃食管交界处腺癌患者。患者按2:2:1的比例随机分配至三组:
A组(352例):卡瑞利珠单抗+CAPOX诱导治疗4-6周期,随后卡瑞利珠单抗+阿帕替尼维持治疗
B组(349例):单纯CAPOX化疗(无维持)
C组(177例):卡瑞利珠单抗+CAPOX诱导治疗4-6周期,随后卡瑞利珠单抗单药维持治疗
分层因素包括ECOG PS、腹膜转移、PD-L1 CPS评分。研究的主要终点为总生存期,先比较A组 vs B组在PD-L1阳性人群中的差异,如显著则继续比较全人群。A组 vs C组、C组 vs B组均为探索性分析。
主要结果:免疫联合化疗显著改善生存,维持加用阿帕替尼未获益
患者基线特征
三组患者的基线特征总体均衡。PD-L1 CPS>1的患者比例在A组为64.5%,B组为68.2%,C组为71.8%。所有患者均存在转移性疾病,最常见的转移部位为肝和腹膜。截至2023年6月7日,中位随访时间在A组为13.5个月,B组为12.1个月,C组为13.7个月。
免疫+化疗 vs 单纯化疗:生存优势明确
中位随访13.5个月,在PD-L1 CPS≥1的人群中:A组中位OS达15.0个月,B组为12.5个月(HR 0.80,P=0.02);在全人群中(无论PD-L1表达):A组中位OS 13.5个月 vs B组12.1个月(HR 0.80,P=0.004)
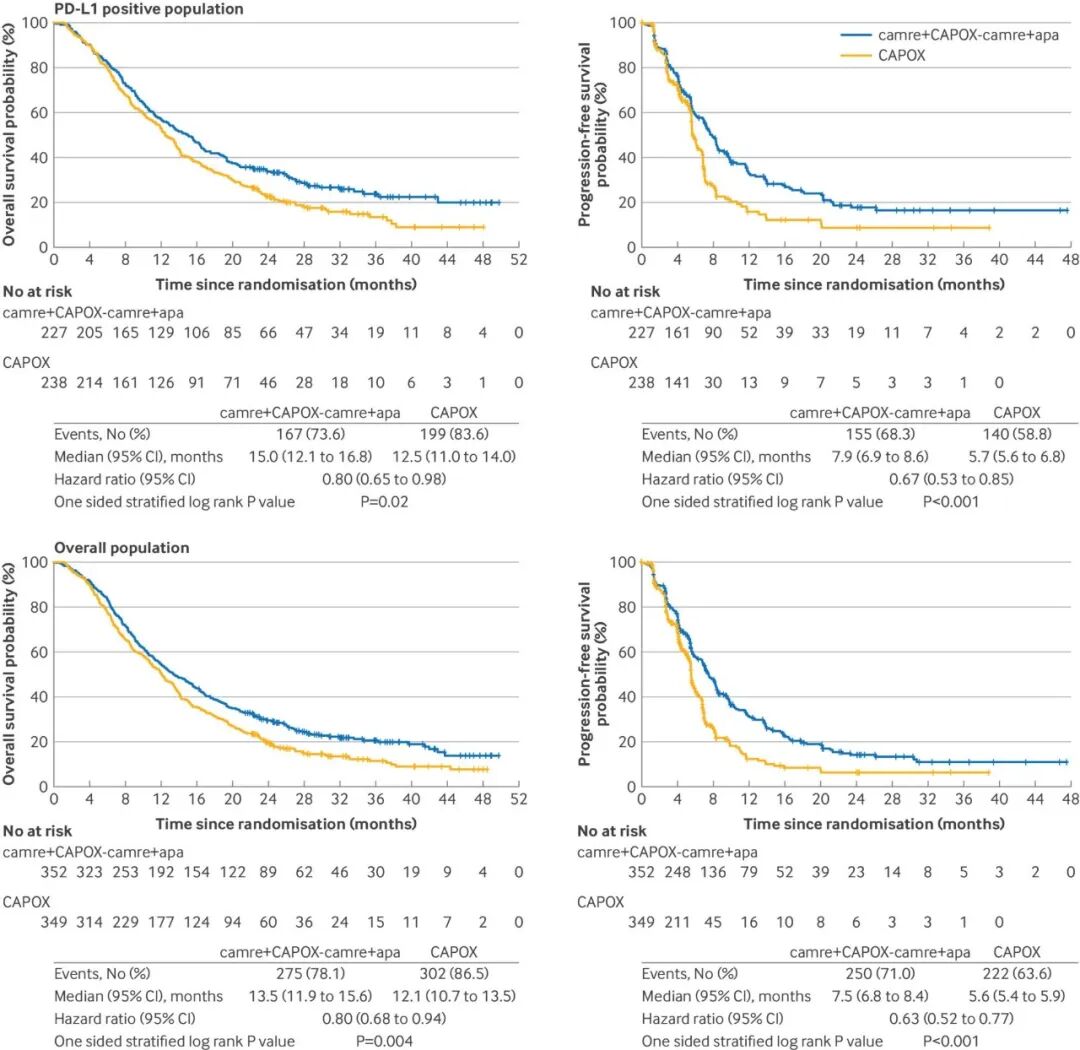
在PD-L1 CPS≥1的人群中:C组中位OS为15.3个月,同样优于B组(HR 0.76,P=0.01);在全人群中(无论PD-L1表达):C组中位OS 14.2个月 vs B组12.1个月(HR 0.80,P=0.02)
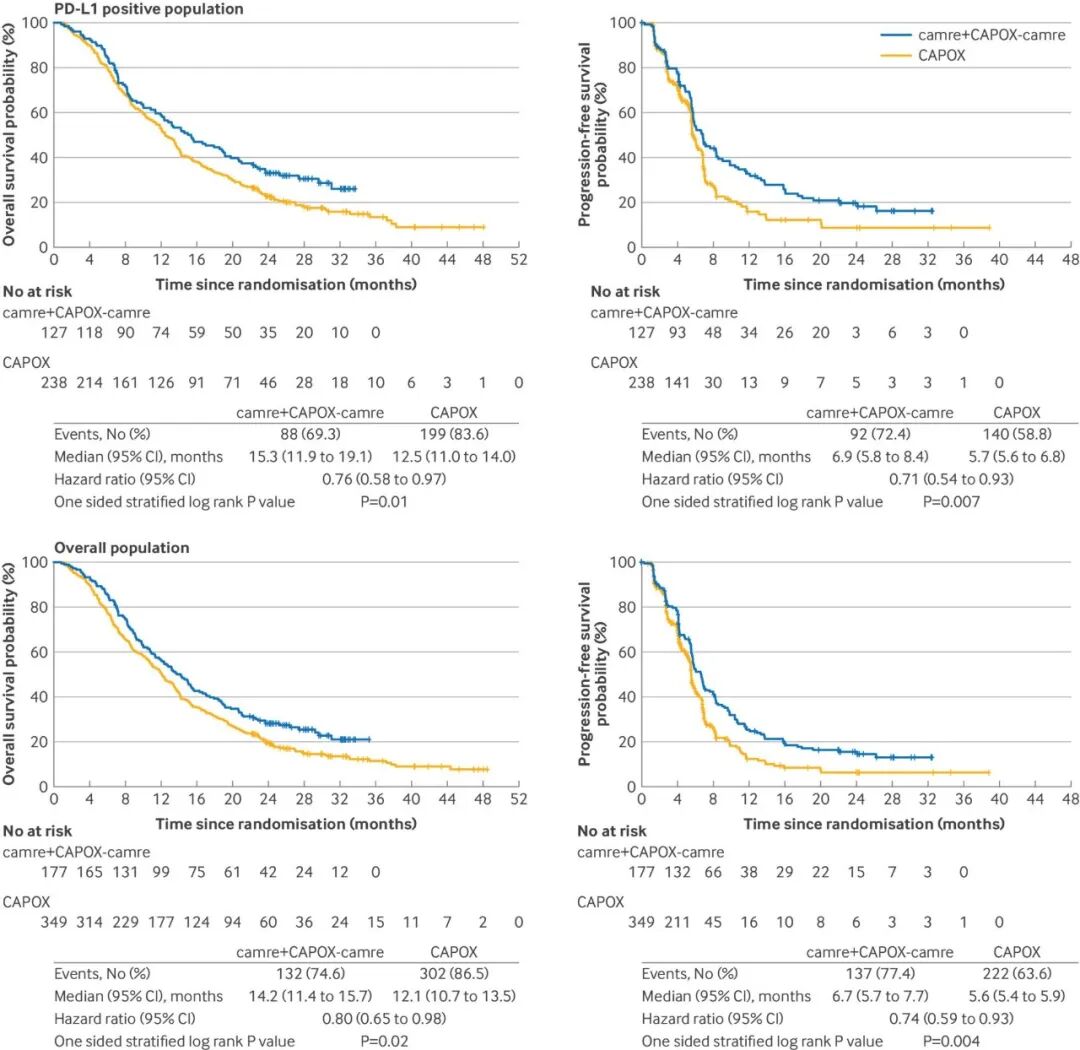
PFS和ORR同样显著改善:A组和C组的ORR分别达57.1%和55.9%,显著高于B组的45.3%;中位DoR也延长至9.0个月和7.0个月,而B组仅5.5个月。
维持治疗是否加用阿帕替尼?
将A组(维持期联合阿帕替尼)与C组(维持期单药)进行探索性比较,结果令人深思:
-OS无差异:HR 1.02(95%CI 0.82–1.26),P=0.45
-PFS无差异:HR 0.92(95%CI 0.74–1.15),P=0.23
-ORR相近:57.1% vs 55.9%
安全性天平明显倾斜:
-≥3级治疗相关不良事件:A组67.9%,远高于B组45.3%和C组46.9%
-治疗相关严重不良事件:A组35.8%,B组15.2%,C组20.9%
-因AE停药率:A组23.0%,B组6.0%,C组10.2%
-治疗相关死亡:A组10例(2.8%),B组3例(0.9%),C组3例(1.7%)
尤其在高血压、蛋白尿、肝酶升高等与VEGFR抑制相关的AE上,A组发生率显著增高。
讨论:加用阿帕替尼为什么未能增效?
本研究结果与CheckMate 649、KEYNOTE-859等研究一致,再次确认了PD-1抑制剂联合化疗在HER2阴性晚期胃癌一线治疗中的核心地位。卡瑞利珠单抗联合CAPOX方案可将死亡风险降低20%,且无论PD-L1表达水平均观察到获益趋势(尽管低表达人群HR置信区间较宽)。
更引人关注的是维持治疗阶段的阴性结果。为何在免疫维持基础上加用阿帕替尼未能锦上添花?可能原因包括:
1. 获益主要来自诱导期:大多数客观缓解在诱导期(卡瑞利珠+CAPOX)即已实现,两组ORR相当,提示阿帕替尼在维持阶段未能进一步缩瘤。
2. 毒性抵消获益:≥3级AE增加可能影响治疗依从性和生活质量,导致部分患者提前停药,削弱了潜在生存优势。
3. 机制重叠或拮抗:尽管临床前研究提示协同,但VEGFR抑制剂对肿瘤免疫微环境的复杂调控可能并非在所有患者中均表现为增强免疫应答。
4. 人群未经选择:阿帕替尼的获益可能仅限于特定亚群(如高VEGF表达、免疫“冷”肿瘤等),但本研究未进行相关生物标志物探索。
研究意义与临床启示
这项III期研究首次在大样本中系统比较了HER2阴性晚期胃癌一线免疫联合化疗后不同维持治疗策略的疗效与安全性。研究证实,无论后续维持方案如何,卡瑞利珠单抗联合CAPOX诱导治疗后继续免疫维持治疗,相比单纯化疗都能显著改善患者的总生存期和无进展生存期。
值得注意的是,在两种卡瑞利珠单抗为基础的维持方案比较中,添加阿帕替尼并未带来额外的生存获益,反而显著增加了≥3级不良事件、治疗中断率和治疗相关死亡率。这一发现在临床实践中具有重要意义:对于大多数未经选择的患者,卡瑞利珠单抗单药维持可能已经达到疗效与安全性的最佳平衡。
研究的结果与CheckMate 649、KEYNOTE-859、ORIENT-16和RATIONALE-305等关键研究一致,在这些研究中,在化疗基础上加入PD-1抑制剂可将死亡风险降低20-23%(中位总生存期13.0-15.2个月 vs 11.4-12.9个月)。在PD-L1阳性人群中,本研究中两种卡瑞利珠单抗方案将死亡风险降低20%和24%(中位总生存期15.0和15.3个月 vs 12.5个月),与CheckMate 649(23%)和KEYNOTE-859(26%)报告的获益幅度相当。这些数据共同强化了免疫检查点抑制剂联合化疗作为HER2阴性胃癌标准一线治疗的地位,并支持卡瑞利珠单抗作为这一领域有效的PD-1抑制剂选择。
研究也为胃癌免疫化疗后维持治疗策略提供了迄今最直接的比较数据。在同期随机患者中,两种卡瑞利珠单抗维持方案的总生存期和无进展生存期相似,而添加阿帕替尼增加了毒性。值得注意的是,大部分客观反应发生在卡瑞利珠单抗联合CAPOX诱导治疗期间,两组反应率相当,提示维持治疗阶段加强抗血管生成治疗并未转化为有临床意义的生存优势。
在当前临床实践中,免疫联合化疗已成为标准一线治疗,本研究的发现对于优化后续维持治疗策略具有直接指导价值。对于大多数患者,卡瑞利珠单抗单药维持可能提供了更有利的获益-风险平衡。
结语
研究证实,对于HER2阴性、不可切除的局部晚期或转移性胃癌或胃食管交界处腺癌患者,无论PD-L1表达状态如何,卡瑞利珠单抗联合CAPOX诱导治疗后继续卡瑞利珠单抗维持治疗相比单纯化疗可显著改善总生存期。在维持治疗阶段添加阿帕替尼未进一步延长生存,但增加了≥3级毒性、治疗中断率和治疗相关死亡率。这些发现表明,相比单纯化疗的生存获益主要来自卡瑞利珠单抗,在未经选择的患者中常规加强维持治疗可能并不合理。未来的研究应明确免疫检查点抑制剂与抗血管生成药物联合的最佳时机、患者选择和用药顺序,并纳入生活质量数据和生物标志物分析,以优化个体化治疗策略。
这项由北京大学肿瘤医院沈琳教授团队领衔的III期研究,不仅为中国原研药物在胃癌领域应用再添高级别证据,也为全球胃癌治疗实践提供了重要参考。在精准医疗时代,“加法”不一定带来更好结局,有时“恰到好处”的减法,才是对患者最大的负责。期待未来更多基于生物标志物的分层研究,为每一位胃癌患者找到最合适的治疗路径。
参考文献:Peng Z, Zhang Y, Xu H, et al. Camelrizumab plus CAPOX with camelrizumab based maintenance versus CAPOX alone as initial treatment for gastric or gastro-oesophageal junction adenocarcinoma: randomised phase 3 trial. BMJ 2026;392:e086115.