ADC之后,抗体偶联寡核苷酸正在崛起

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效
当抗体偶联药物(ADC)不断刷新癌症治疗边界之际,一种新的偶联药物形式也正在快速走入行业视野。近日,Nature Biotechnology上发表的一篇文章指出,抗体偶联寡核苷酸(antibody–oligonucleotide conjugates,AOCs)正在成为值得关注的创新治疗模式。

报道提到,2025年10月,诺华(Novartis)以120亿美元收购Avidity Biosciences,将这一治疗模式推向资本与产业焦点。多个AOC项目已进入3期临床开发或准备提交生物制品许可申请(BLA),尤其是在杜氏肌营养不良症(DMD)领域,首批产品已逼近监管节点。
靶向肝外组织:递送版图正在扩展
过去十年,寡核苷酸药物的成功高度集中在肝脏适应症。Alnylam等公司通过GalNAc偶联技术实现了对肝细胞的高效递送,带动了siRNA与反义寡核苷酸(ASO)药物的快速发展。但当治疗靶点转向肌肉、心脏、中枢神经系统(CNS)等组织时,问题开始变得复杂。血脑屏障、组织屏障结构、受体分布差异,使“肝外递送”成为核酸药物领域需要解决的重大挑战之一。
AOC正是在这一背景下涌现的创新递送技术。通过将寡核苷酸与抗体偶联,利用抗体识别特定受体,例如转铁蛋白受体1(TfR1),实现组织选择性递送,Avidity Biosciences与Dyne Therapeutics等公司率先在DMD领域取得突破。临床数据显示,抗体偶联策略显著提升了肌肉组织中的肌营养不良蛋白(dystrophin)的表达水平,相较非偶联ASO呈现数量级提升。
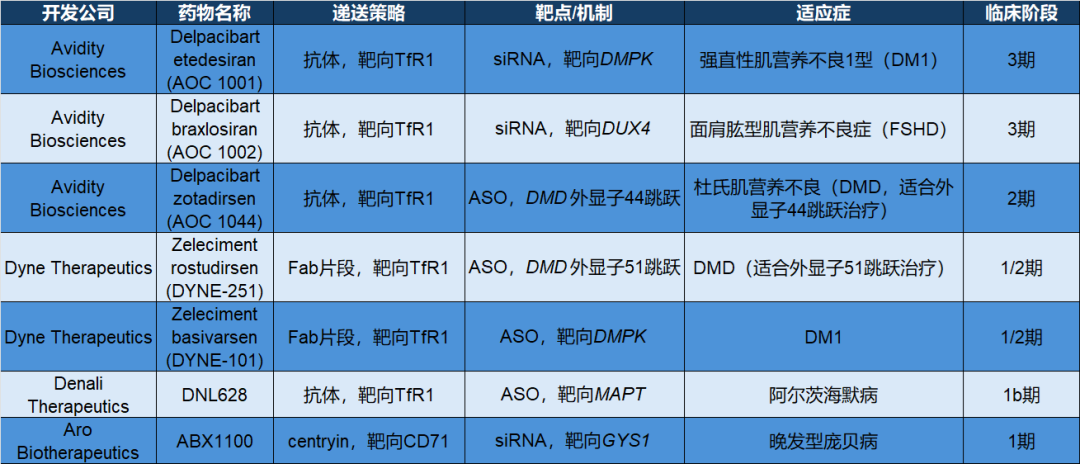
▲部分临床期在研抗体偶联寡核苷酸疗法(数据来源:参考资料[1])
与此同时,多肽偶联寡核苷酸(peptide–oligonucleotide conjugates,POCs)也快速推进。Entrada、PepGen等公司利用细胞穿透肽或环肽增强寡核苷酸的胞内转运与内体逃逸效率,在肌肉、心脏以及CNS方向展开探索。部分候选药物在临床中显示出远高于传统寡核苷酸的剪接纠正或基因沉默效果。可以说,偶联策略正在重塑寡核苷酸药物的递送逻辑。
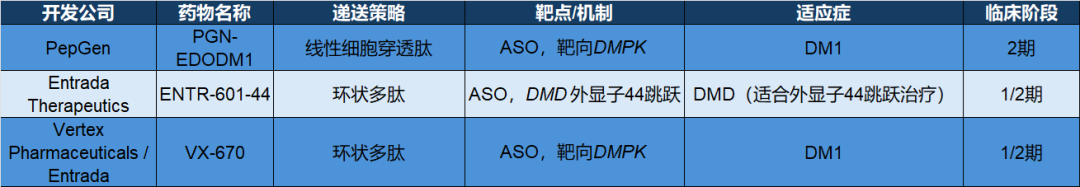
▲部分临床期在研多肽偶联寡核苷酸疗法(数据来源:参考资料[1])
递送突破之后:复杂偶联分子的下一个挑战
然而,递送能力的提升只是第一步。当抗体、多肽、连接子与寡核苷酸整合为一个偶联分子后,其体内行为远比单一药物形态更为复杂。
AOC在体内可能以多种分子形式存在:完整偶联体、部分降解偶联体、游离寡核苷酸、降解片段等。抗体部分影响循环半衰期与组织分布,连接子决定稳定性及释放节奏,而寡核苷酸部分则涉及胞内摄取、内体逃逸与功能表达。
因此,影响偶联寡核苷酸药物转化成功率的因素,不仅是递送技术的创新,也需要对药物在患者体内命运的系统理解和精准解析。在这一阶段,针对偶联寡核苷酸药物代谢和药代动力学(DMPK)研究的重要性显著提升。
对于AOC而言,需要回答一系列关键问题:
偶联药物在体内的完整性如何?
连接子是否在目标组织前提前断裂?
游离寡核苷酸的暴露水平与药效是否相关?
是否存在非预期组织分布?
不同偶联位点设计是否影响药代动力学(PK)特征?
暴露–效应关系是否具备可预测性?
围绕这些问题,系统化的体外ADME研究、体内PK评价与多组分生物分析能力,正在成为偶联寡核苷酸药物研发的重要技术基础。
一体化平台助力抗体偶联寡核苷酸药物开发
围绕AOC这一复杂分子形式,药明康德DMPK团队建立了覆盖体外ADME研究、体内PK评价及生物分析方法开发的系统化能力体系,可针对AOC由抗体、连接子与寡核苷酸三部分构成所带来的多维度代谢与分布挑战,设计匹配的研究策略。基于对AOC结构特征与ADME行为关系的深入理解,团队能够支持代谢物鉴定、暴露-效应关系分析以及PK研究方案优化,并为连接子类型选择、偶联位点设计及寡核苷酸修饰策略提供数据支持,从而在体内稳定性、靶向递送与细胞内释放之间实现平衡。
依托跨平台检测技术与寡核苷酸DMPK研究经验的协同整合,该能力不仅能够解析AOC在ADME过程中的关键行为特征,也可贯穿发现、临床前及临床阶段,为客户在新型偶联药物开发中提供兼具科学深度与转化导向的一体化DMPK解决方案,加速复杂新分子从机制验证迈向临床转化。
AOC与POC的未来
Nature Biotechnology的文章表示,展望未来,偶联寡核苷酸领域将在递送技术和载荷化学方向继续推进。现有偶联寡核苷酸药物广泛使用TfR1作为靶向递送的受体,然而多家公司已经在探索基于更具特异性的受体的递送技术。例如,Manifold Bio公司正在通过体内筛选技术,发现用于递送抗体或寡核苷酸的新特异性受体。该公司已与罗氏(Roche)达成超过20亿美元的研发合作,开发用于治疗神经系统疾病的递送技术。
在优化载荷方面,渤健(Biogen)公司的新一代ASO疗法salanersen采用了新的化学修饰。而City Therapeutics也在开发基于诱导切割微RNAs(cleavage-inducing tiny RNAs)的创新疗法,目的是获得更强效的RNA干扰效应。
随着抗体与寡核苷酸、多肽与siRNA不断组合,分子复杂度持续上升,对药物体内命运进行系统化、定量化、可预测化解析的DMPK能力正成为支持转化决策的重要一环。药明康德将持续依托其一体化服务平台,助力包括AOC和POC在内的偶联寡核苷酸疗法的开发,让突破性技术早日转化为造福全球病患的创新疗法。
参考资料:
[1] Sheridan (2026) Now with oligos: antibody–oligonucleotide conjugates are the new drug modality to watch. Nat Biotechnol, https://doi.org/10.1038/s41587-025-02987-0
免责声明:本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。
分享,点赞,在看,聚焦全球生物医药健康创新

