最新!CDE新增1条受理共性问题

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效

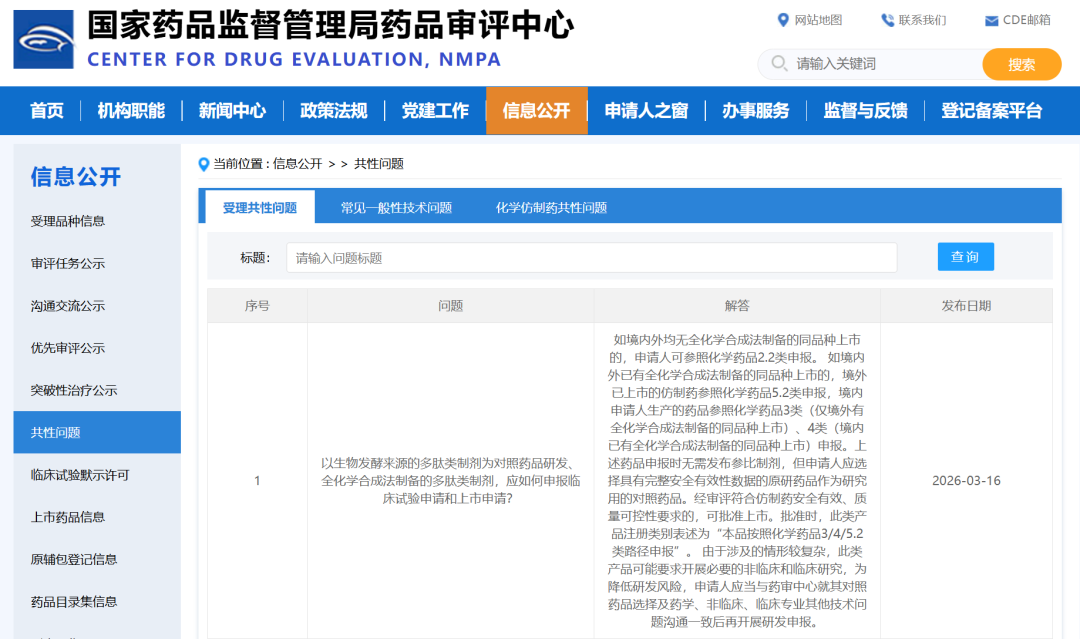
3月16日CDE更新1条受理共性问题
01
以生物发酵来源的多肽类制剂为对照药品研发、全化学合成法制备的多肽类制剂,应如何申报临床试验申请和上市申请?
答
如境内外均无全化学合成法制备的同品种上市的,申请人可参照化学药品2.2类申报。 如境内外已有全化学合成法制备的同品种上市的,境外已上市的仿制药参照化学药品5.2类申报,境内申请人生产的药品参照化学药品3类(仅境外有全化学合成法制备的同品种上市)、4类(境内已有全化学合成法制备的同品种上市)申报。上述药品申报时无需发布参比制剂,但申请人应选择具有完整安全有效性数据的原研药品作为研究用的对照药品。经审评符合仿制药安全有效、质量可控性要求的,可批准上市。批准时,此类产品注册类别表述为“本品按照化学药品3/4/5.2类路径申报”。 由于涉及的情形较复杂,此类产品可能要求开展必要的非临床和临床研究,为降低研发风险,申请人应当与药审中心就其对照药品选择及药学、非临床、临床专业其他技术问题沟通一致后再开展研发申报。
-END-

2026药典符合性实验室管理和分析方法验证及数据统计分析专题研讨班
时间:2026年03月26日-28日
地点:上海市
课程背景与目标
课程时间安排
03月27日 9:00-12:00 13:30-16:30
符合2025版药典的实验室规范化管理
一、实验室质量管理法规体系概述
二、符合2025版药典的药品检验流程管理
1.人员培训和资质确认(职责及培训计划、上岗前培训与资质确认、培训档案管理)
2.2025版药典:药品取样全流程合规要点(风险控制点:环境、工具、交叉污染)
3.样品管理(法规、转运和接受、储存与发放)
4.2025版药典《9094分析仪器确证指导原则》:基于风险评价分析仪器分类管理与生命周期管理(分析仪器分类、编号管理、校验与维护)
5.通则《0291国家药品标准物质通则》、通则《9901国家药品标准物质研制指导原则》增修订内容及实施要点
a通则0291 国家药品标准物质通则修订及实施转化解读
b通则9901国家药品标准物质研制指导原则修订及实施转化解读
药典凡例与药典符合性检验技术操作规范
一、2025版药典凡例深度解读与合规应用
1.凡例的法律地位与核心作用(作为药典标准解读的“纲领性文件”,指导检验全流程)
2.药典凡例法定约束力边界
3.术语定义(如 “精密称定”“恒重”“澄清” 等术语的量化标准与操作边界)
4.标准表述规则(如“不得过”“应符合规定” 等表述的合规判定逻辑)
二、药典核心检验方法原理与与符合性操作
1.常用物理常数测定方法(熔点、沸点、比旋度)的药典要求与操作规范
2.鉴别试验方法实操要点标准操作
3.杂质检查方法核心原理,如杂质限量计算、外标法/内标法应用场景,有关物质检测的色谱
4.含量测定方法分类解析,容量分析法、紫外分光光度法、色谱法的适用范围与选择逻辑。
主讲人:张老师
03月28日 9:00-12:00 13:30-16:30
一、基于ICHQ2(R2)、中国药典9101与USP1225的分析方法验证综合考量
1)方法验证基本要求
1 分析方法验证适用范围
2.分析方法的生命周期管理
3 可报告范围确定
4 稳定性指示方法
5 多变量分析方法
2)分析方法验证的主要内容及关键要点
1专属性评估,多种方法验证方法的专属性
2准确度实验设计原则和可接受标准
3精密度实验设计原则和可接受标准
4 工作范围确定
4.1 校准模型建立 线性或非线性和范围设计的基本原则
4.2 低范围限的验证,检测限和定量限的评估
5方法耐用性的设计和评价
6系统适用性试验的选择
分析方法评价和使用中的统计学工具
一、测量不确定度及其应用
1.测量不确定度的应用
●计量认证、计量确认、质量认证和实验室认可
●参加能力验证、或国际间实验比对活动
●标准物质标定
●仪器校准和检定
●判定检测结果符合性,特别对临界值的判断时
●其它情况,如客户有要求时
2.检测结果符合性评价
3.置信区间的确定-案例剖析
二、异常值的检验与剔除(USP<1010>)
1.什么样的数据必须剔除?
2.几种常用判别分析异常数据的统计方法?
●拉依塔准则
●格罗布斯准则
●狄克逊准则
三、分析结果的比较
1.分析结果比对要点
●人员比对●仪器比对●方法比对
●标准物质比对●留样再试●实验室间比对
2.统计分析比对试验结果方法
●F检验法(USP推荐方法)
●T检验法(USP推荐方法)
●En值判断法
●CD值判断法
●允差判断法
●Z比分数
●F检验法的案例分析
四、Horwitz方程及其应用
1.实验室间数据偏差评价
2.Horwitz方程在比对试验质量评估中的应用
五、如何评价分析方法的准确度和精密度(USP<1210>)
(1)基于测量不确定度的考虑
(2)常量分析方法回收率置信区间
(3)精密度的置信区间
(4)微量分析方法置信区间
(5)准确度与精密度的联合验证
六、检测限和定量限的评估新方法(USP<1210>)
主讲人:王老师
会务费
培训费:4800元/单位,每单位限额3人(1600元/人),包含(专家费、资料费、场地费、现场问答等)。食宿统一安排,费用自理。
培训报名联系人:王老师
微信/手机:155 0614 0531

扫码添加微信
【点这里,进入医药数据库,搜索下载原文】

药学检测服务推荐
一、化药检测服务
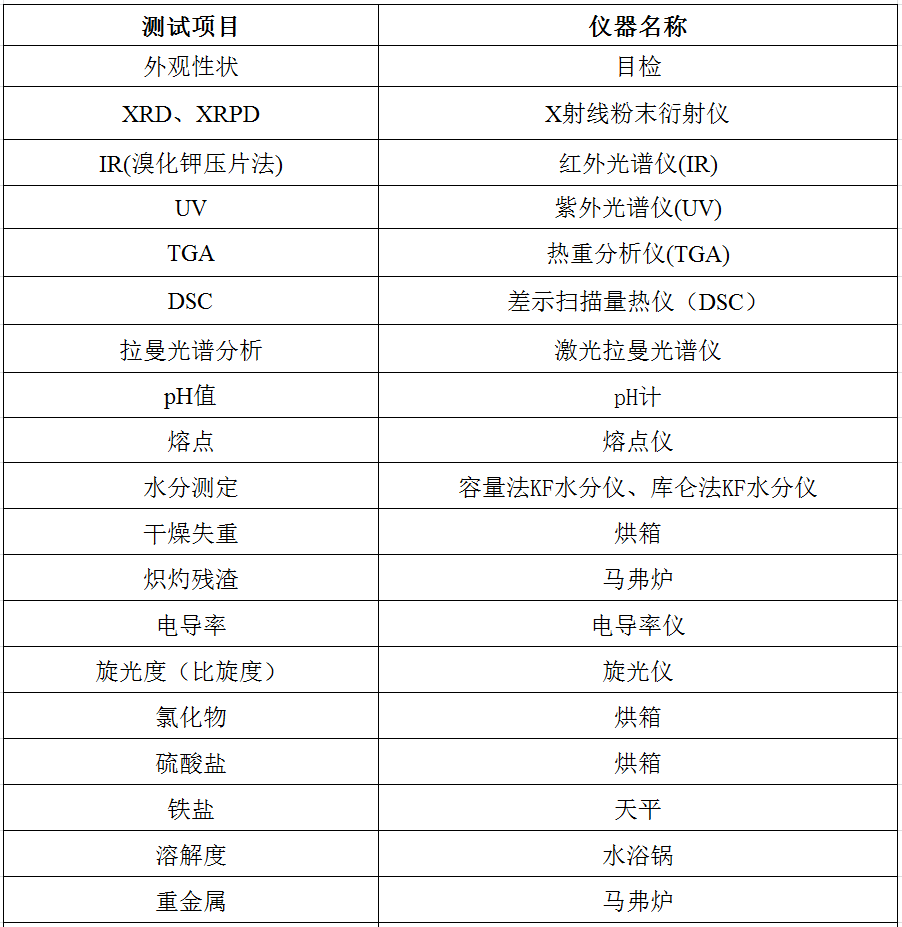



二、化药质量研究服务
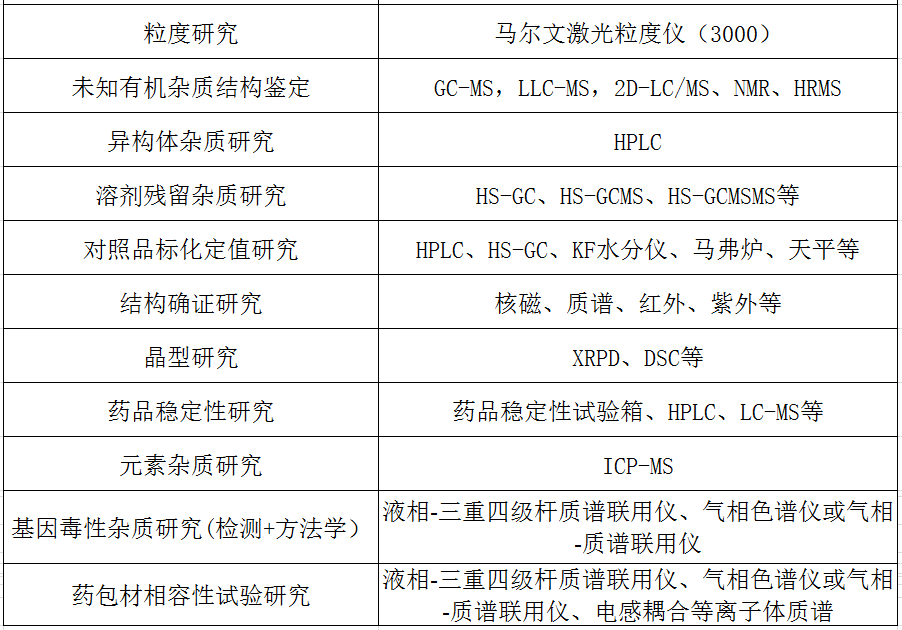

三、生物药检测服务

四、生物药质量研究服务
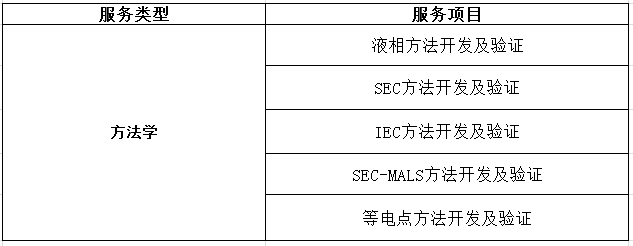
五、药品毒理安全性评价服务

六、药品包装材料理化检测
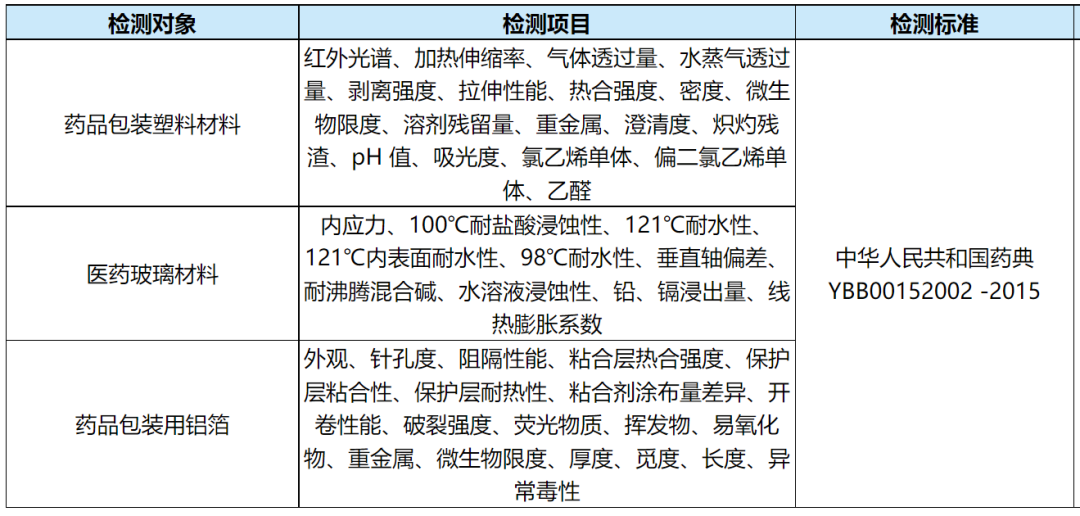
实验室资质:CMA、CNAS
实验室所在地:上海、苏州、青岛、广州、福州
联系我们:151-9002-7486/181-0068-0718(微信同号)


文章来源:科威利华,本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的单位、媒体或个人可与我们联系(274190388@qq.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。



