Science:打破恶性循环!肾脏损伤如何“喂养”肠道细菌,使其释放毒素加速肾病恶化

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效
加州大学戴维斯分校医学院的研究人员揭示了失衡的肠道微生物组如何加剧某些肠道细菌代谢副产物的产生。这种失衡驱动了一个使小鼠慢性肾病(chronic kidney disease, CKD)恶化的反馈循环。科学家们确定了一种可能打破这一破坏性循环的在研药物。该研究发表在《科学》杂志上。

研究团队证明,肾功能损伤会增加结肠中的硝酸盐水平。硝酸盐为大肠杆菌(
E. coli
)产生吲哚提供了助力,吲哚是一种有机化合物,会转化为有害废物——硫酸吲哚酚,从而进一步损害肾脏。阻断肠道中一种单一酶——诱导型一氧化氮合酶(inducible nitric oxide synthase, iNOS)的产生,就能够阻止这一破坏性循环。
"先前的研究已表明,慢性肾病与粪便中肠杆菌科细菌的丰度升高有关。"该研究的第一作者、医学微生物学与
免疫
学系项目科学家 Jee-Yon Lee 说。
肠杆菌科(Enterobacteriaceae )是一个庞大的细菌家族,包括无害和致病物种。"这项研究将宿主的硝酸盐确定为一种开关,能将大肠杆菌等常见肠道细菌转化为能够加速慢性肾病的吲哚生产者。"Lee 说。
美国约有七分之一的成年人患有慢性肾病
慢性肾病是一种肾功能逐渐丧失的疾病,影响着美国约七分之一的成年人,估计有3550万美国人。大约三分之一的
糖尿病
患者和五分之一的
高血压
患者患有肾脏疾病。据估计,2023年全球约有7.88亿人患有慢性肾病。
对于
肾衰竭
患者来说,血液透析是一种从血液中清除废物和多余液体的救命方法。但硫酸吲哚酚无法通过透析清除,因为它会与血清白蛋白结合。较高的血清硫酸吲哚酚水平与更严重的慢性肾病相关。
"通过识别导致慢性肾病期间肠杆菌科细菌增加的驱动因素,并通过证明这些细菌对吲哚产生和疾病进展的重要性,我们的研究指出 iNOS 是干预策略的一个潜在靶点。"该论文的资深作者、医学微生物学与免疫学系杰出教授 Andreas Bäumler 说。
方法与可能的疗法
研究人员在小鼠中测试了特定的大肠杆菌菌株。他们还测试了患有和未患有慢性肾病的人的粪便样本。他们在小鼠中发现:(1)肾
功能障碍
导致结肠粘液层中 Nos2 (即负责产生iNOS的基因)的转录增加;(2)iNOS 的增加导致一氧化氮增加,一氧化氮与氧自由基反应形成硝酸盐;(3)硝酸盐水平升高促进了大肠杆菌的生长,导致肾脏毒素硫酸吲哚酚的产生增加,形成了破坏性的反馈循环。
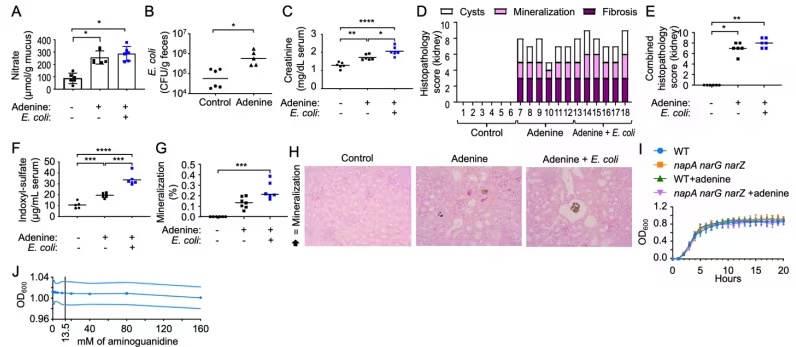
除了小鼠的发现,研究人员还发现
慢性肾病患者
的粪便样本显示出与小鼠相同的效应。尽管肾病患者的粪便样本显示出更高水平的大肠杆菌,但与健康对照组相比,只有在添加硝酸盐后,吲哚的产生才会增加。
为了确定降低 iNOS 水平是否能改善小鼠的预后,研究人员测试了氨基胍,一种已知能抑制 iNOS 的在研药物。给予氨基胍的小鼠表现出粘膜硝酸盐减少、硫酸吲哚酚降低和肾脏结局改善。
局限性与下一步
尽管这些结果对于找到一种减少硫酸吲哚酚的机制,并可能改善肾病的进展很有希望,但研究人员指出了几个局限性。
尽管人类肠道细菌在小鼠中反映出了硝酸盐依赖性的吲哚激增,但仍需更多研究来证实这些结果在人类中的适用性。还需要进行临床试验来测试 iNOS 抑制剂或其他激动剂或抑制剂是否能安全地降低硫酸吲哚酚并改善慢性肾病患者的预后。
最后,他们指出肠道生态系统是复杂的。大肠杆菌并非唯一产生吲哚的肠道细菌,长期抑制硝酸盐途径可能会带来未知的权衡。
"这项研究表明,改变肠道环境——而不仅仅是微生物本身,可以对疾病进展产生深远影响。"Bäumler 说。"靶向塑造微生物代谢的宿主通路,可能代表了干预慢性肾病的一种新方法。"(
生物谷
Bioon.com)
参考文献:
Jee-Yon Lee et al,
Host-derived nitrate fuels indole production by Escherichia coli to drive chronic kidney disease progression
, Science (2026). DOI: 10.1126/science.ady5217.

