Nature:大规模基因研究厘清EBV致病机制——高病毒载量直接引发霍奇金淋巴瘤,但与多发性硬化症关联源于免疫反应异常,非病毒本身

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效
许多病毒已经适应在感染者的体内长期存活。当人体感染病毒后,体内病毒复制与抗病毒免疫识别之间的长期平衡可能会导致病毒自然清除、病毒载量维持在一个稳定的水平(类似于终身的 EBV 感染情况),或者发展为疾病(例如从人类免疫缺陷病毒(HIV)感染发展为获得性免疫缺陷综合征(AIDS))。EBV 感染在初次感染多年后是霍奇金淋巴瘤和多发性硬化症的显著风险因素,并且与一些自身免疫性疾病有关,但其具体原因尚不明确。

2026年3月25日,哈佛医学院Po-Ru Loh团队在
Nature
在线发表题为
“The DNA virome varies with human genes and environments”
的研究论文,该研究利用来自UK Biobank(n = 490,401)、“All of Us”(n = 414,817)和西蒙斯基金会推动自闭症研究知识项目(Simons Foundation Powering Autism Research for Knowledge)(SPARK;n = 12,519)的全基因组测序数据,分析了 31 种常见病毒在人类血液和唾液中的病毒 DNA 载量。
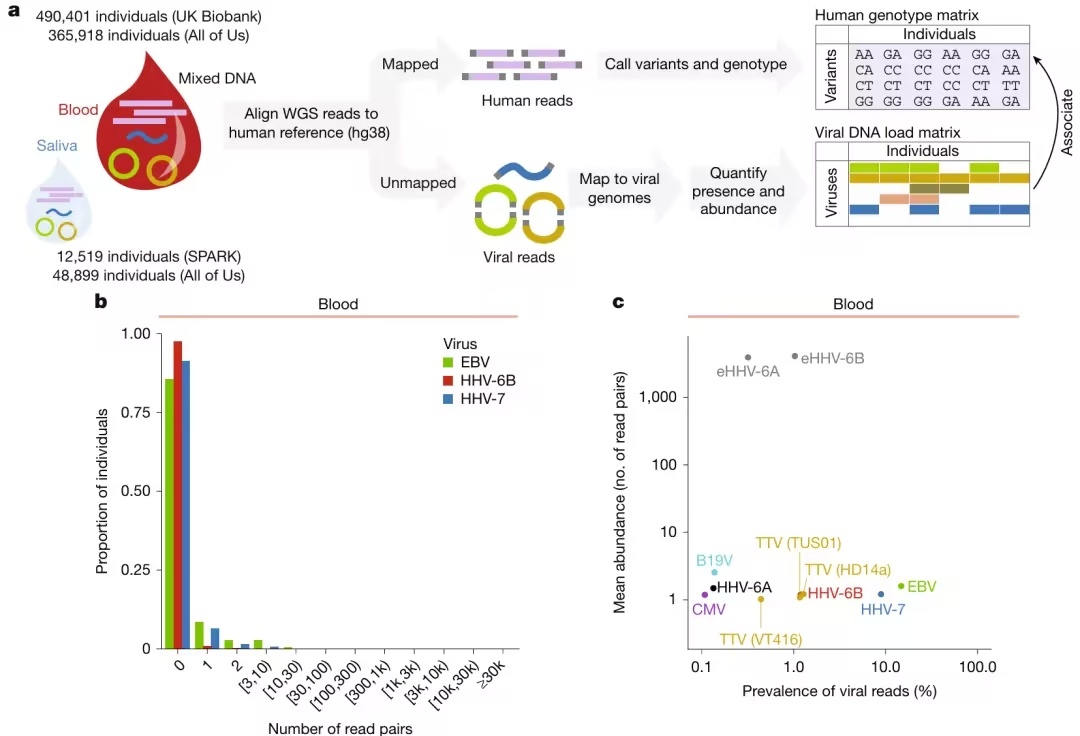
血液和唾液中病毒 DNA 载量的检测与定量 WGS(图源自
Nature
)
病毒 DNA 载量随年龄、一天中的时间以及季节而显著变化;大多数病毒在男性体内的含量也高于女性。在与七种病毒的 DNA 载量相关的几十个位点上存在人类遗传变异:Epstein–Barr(EBV,45 个位点)、人类疱疹病毒(HHV)-7(37 个位点)、HHV-6B、Merkel细胞多瘤病毒和三种环状病毒。在主要组织相容性复合体(MHC)位点的变异产生了最强的关联(P = 5.8 × 10–9 至 2.5 × 10–1499),这些关联对于每种病毒都是特定的。
HLA-B*08:01 等位基因还与 EBV 亚型表现出宿主-病毒的遗传相互作用(P = 7.4 × 10
–70
)。其他人类遗传因素还涉及编码用于抗原呈递的肽类物质加工蛋白的基因,例如 ERAP1(HHV-7,P = 2.7×10
–78
)和 ERAP2(EBV,P = 4.6×10
–111
)。孟德尔随机化分析证实,EBV DNA 载量与霍奇金淋巴瘤风险增加之间存在显著的因果关系(P = 1.8×10
–3
),但与多发性硬化症则无此关联(P = 0.52)。这表明,长期的慢性 EBV 感染会增加淋巴瘤风险,而 EBV 感染与自身免疫性疾病之间的关联反映了宿主对特定病毒表位的免疫反应。
参考消息:https://www.nature.com/articles/s41586-026-10288-y

