Eur Heart J:华中科技大学董念国等揭示衰老相关代谢转变加重钙化性主动脉瓣膜病新机制

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效
钙化性主动脉瓣疾病缺乏有效的药物治疗,并且与衰老密切相关。由于烟酰胺腺嘌呤二核苷酸(NAD+)随着年龄的增长而稳步下降,NAD+补救代谢的细胞类型特异性破坏是否驱动瓣膜炎症和钙化。
2026年3月17日,华中科技大学董念国、李飞、昆明医科大学Zhu Da、浙江大学蔡哲钧共同通讯在
European Heart Journal
在线发表题为
“Senescence-associated metabolic alterations aggravate calcific aortic valve disease”
的研究论文。该研究表明衰老相关的代谢改变加重钙化性主动脉瓣疾病。
钙化性主动脉瓣疾病由内皮NAD+不足引发,并被代谢多样的巨噬细胞放大。这种分隔的NAD+回路将炎症与基质突变耦合起来。通过烟酰胺单核苷酸的早期NAD+补充和针对NAMPT的干预保证了作为钙化性主动脉瓣疾病潜在疗法的临床评估。

钙化性主动脉瓣疾病(CAVD)已经成为一种主要的年龄相关心血管流行病,影响超过12%的65岁以上的人,并表现为从早期纤维钙化病变到严重主动脉狭窄的渐进转变。随着全球人口老龄化,CAVD是心血管死亡的第三大原因,占心力衰竭病例的10%-20%。在症状发作的2年内死亡率为50%。这种病理级联反应曾被错误地描述为被动的“磨损”退化,现在被认为是一种主动的适应不良过程。
虽然CAVD的致病机制正在逐步得到阐明,但主动脉瓣生物学中与年龄相关的特定变化仍然缺乏特征。衰老研究的最新进展已经确定了共同的特征—包括细胞衰老、慢性炎症和线粒体功能障碍—这些特征驱动了机体衰老和CAVD发病机制。病理特征的这种趋同强调了研究它们之间的机械联系的迫切需要,从而揭示衰老是如何成为CAVD发生的基本催化剂的。
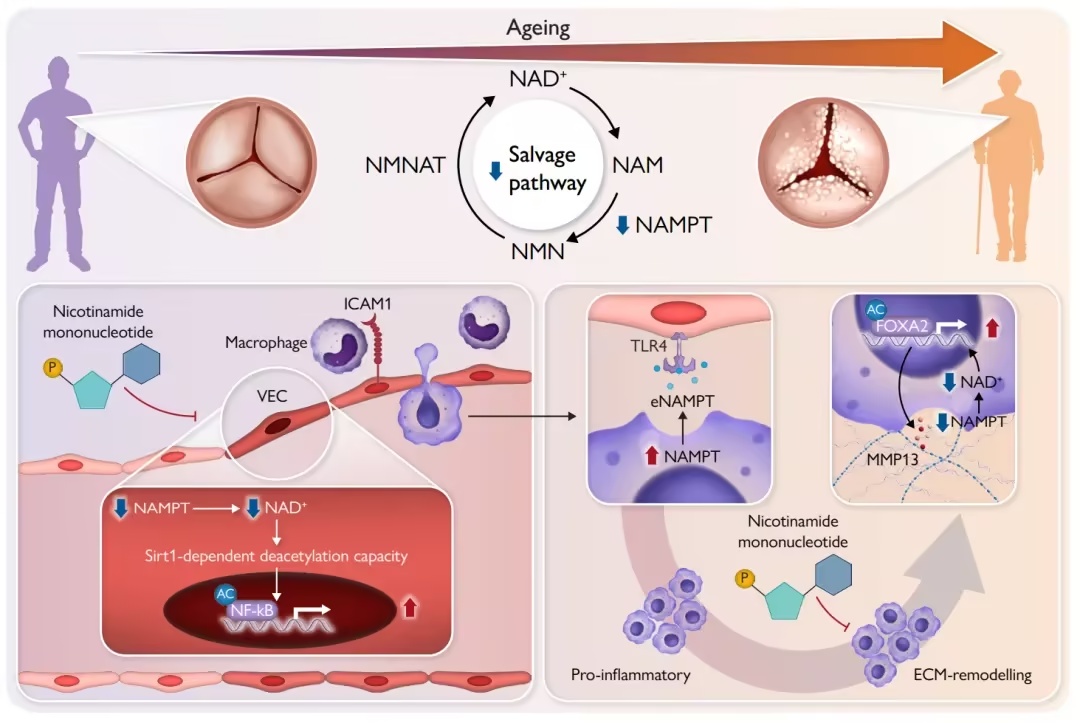
机理模式图(
European Heart Journal
)
在这项研究中,研究人员发现NAMPT介导的补救途径的抑制是老年主动脉瓣的主要代谢重连。在单细胞分辨率下,描绘了瓣膜内皮细胞(VECs)和巨噬细胞之间的异质性NAMPT表达模式,揭示了协调钙化的细胞间串扰。此外,还揭示了巨噬细胞固有的NAMPT异质性在驱动CAVD进展中的双重功能作用——促进前炎症活化和细胞外基质(ECM)重塑。该发现确定内皮NAMPT缺乏是年龄相关CAVD的主要起始因素,其中募集的巨噬细胞通过炎症级联反应和胶原降解。
华中科技大学同济医学院附属协和医院心脏大血管外科董念国教授、李飞教授,浙江大学医学院附属第二医院心血管内科蔡哲钧教授为该论文共同通讯作者;华中科技大学同济医学院附属协和医院心脏大血管外科钱兴宇、徐力、郑一聃、范正锋为该论文的共同第一作者。本工作得到陆军军医大学第二附属医院谢明辉等的大力支持。该研究得到国家自然科学基金优秀青年基金(82322007)、国家自然科学基金面上项目(82300417、82170377)、国家重点研发计划(2022YFC2503401)等多项基金资助。
参考消息:https://doi.org/10.1093/eurheartj/ehag191

