Cell Biomaterials:同济大学李永勇/李艳团队发现纳米力学调控巨噬细胞外泌体分泌新机制及免疫功能重塑

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效
外泌体的生物调控机制对其生物合成、分泌及货物分选过程具有关键调控作用,在细胞间通讯、疾病发病机制及精准医学领域发挥核心作用。然而,纳米力学信号如何调控外泌体分泌机制及其生物学效应仍鲜有研究。
2026年3月6日,同济大学李永勇,李艳共同通讯在
Cell Biomaterials
在线发表题为
Piezo1-mediated regulation of macrophage-derived exosome secretion via nanoparticle elasticity for tumor immunomodulation
的研究论文。

该研究系统性地阐明了纳米颗粒弹性对巨噬细胞外泌体分泌及其免疫功能的调控机制。通过构建具有可调杨氏模量(范围为103.2至1,064.7 MPa)的二氧化硅纳米颗粒(SNs)作为单变量机械系统,定量数据表明:低模量的SNs(20% SNs,103.2 MPa)能显著增强骨髓来源巨噬细胞(BMDMs)的外泌体分泌能力。
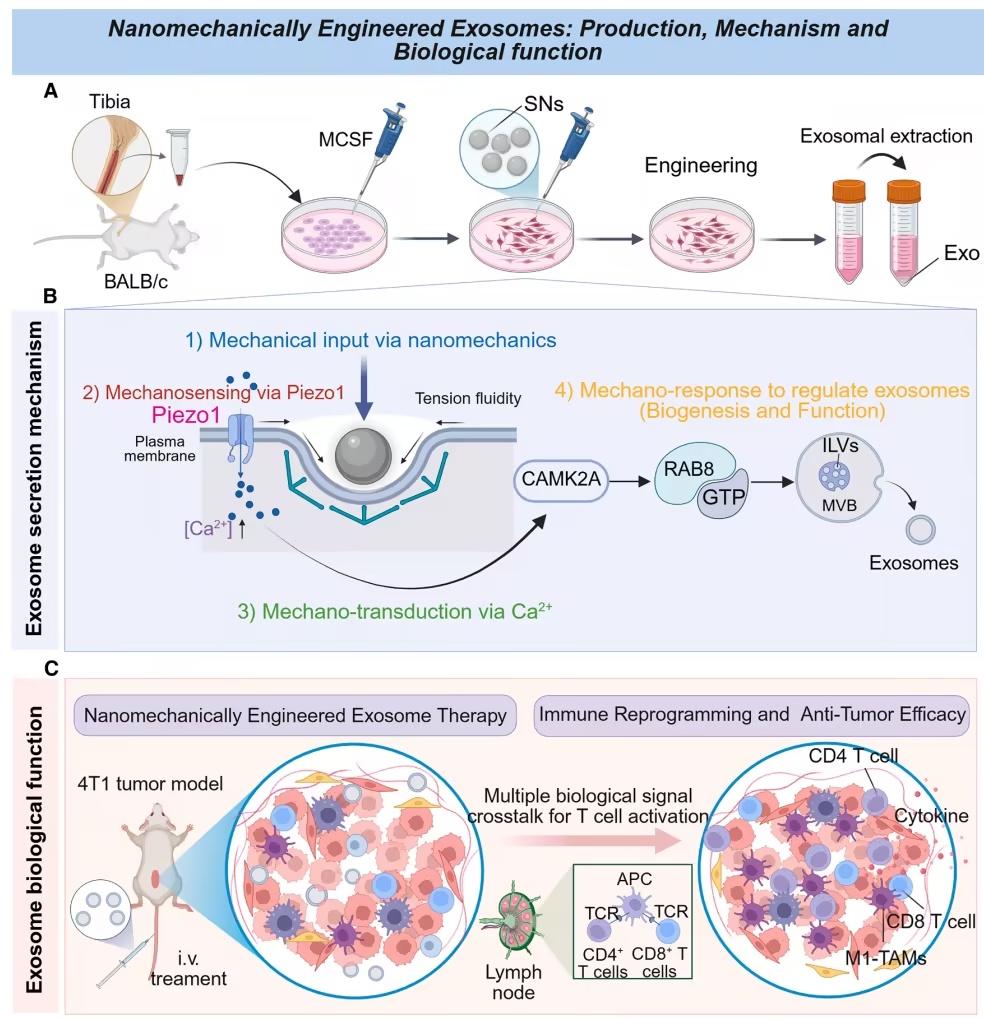
文章模式图(图源自
Cell Biomaterials
)
进一步研究发现,这种机械刺激可促进Piezo1蛋白激活、诱导钙离子内流,并进而触发CAMK2A / GTP-Rab8信号轴。外泌体蛋白质组学分析显示,低模量SNs诱导的巨噬细胞来源外泌体(Exo20% SNs)通过多通路交互作用协同增强T细胞受体信号通路激活,从而加剧促炎反应。
体内抗肿瘤实验表明,与LPS激活的炎症巨噬细胞分泌的外泌体相比,Exo20% SNs能显著抑制肿瘤生长,并伴随免疫抑制性肿瘤微环境的重塑。本研究建立了“纳米力学外泌体工程化”范式,为机械调控外泌体免疫生物学提供了基础性见解,并为精准外泌体治疗学提供了蓝图。
文章链接:https://doi.org/10.1016/j.celbio.2026.100387

