优于司美格鲁肽!诺和诺德/联邦制药三靶点激动剂II期研究成功

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效
2026年3月25日,联邦制药发布公告,其自主研发的1类创新药UBT251注射液在中国2型糖尿病患者中开展的II期临床研究达到预期目标。研究结果显示,这款长效GLP-1/GIP/GCG三靶点受体激动剂在降糖和减重两个核心指标上均显著优于司美格鲁肽,展现出成为同类最优的潜力。
基于这一积极结果,联邦制药将尽快启动中国2型糖尿病患者的III期临床研究,标志着这款国产创新药正加速向市场迈进。

图1. UBT251注射液II期临床研究进展公布,来源:联邦制药官方公告
01
强强联合押注UBT251
UBT251是联邦制药全资附属公司联邦生物科技自主研发的1类创新药,也是中国首家、全球第二家以化学合成多肽法制备的长效GLP-1R/GIPR/GCGR三靶点激动剂获批临床的企业。
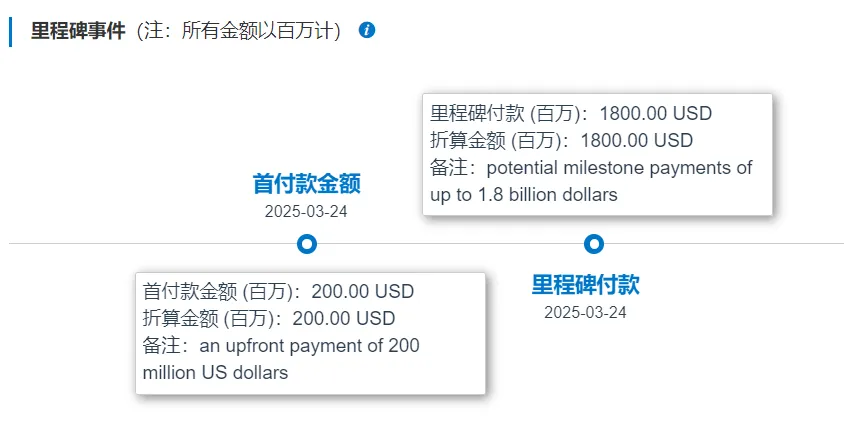
图2. 此次交易里程碑及对应款项,来源:药渡数据-医药交易库
2025年3月,联邦生物科技及联邦制药与诺和诺德股份有限公司就UBT251达成独家许可协议,根据协议,诺和诺德将获得UBT251在全球范围内(不包括中国大陆、香港、澳门和台湾地区)的独家开发、制造和商业化权利。联邦制药保留UBT251在中国大陆、香港、澳门和台湾地区的权利。联邦制药将获得2亿美元的预付款,并有资格获得高达18亿美元的潜在里程碑付款,以及在上述地区以外的净销售额的分级特许权使用费。详情回顾:20亿美金!中国首个代谢领域三重激动剂出海!
这一合作不仅验证了UBT251的临床价值和商业潜力,也为联邦制药的创新药出海开辟了重要通道。
02
GLP-1/GIP/GCG三重机制
UBT251是一款长效GLP-1/GIP/GCG三靶点受体激动剂。其设计理念基于对不同肠促胰岛素和代谢调节激素的深入理解:
GLP-1通过抑制食欲、延缓胃排空实现降糖减重;
GIP在改善胰岛素敏感性、调节脂代谢方面发挥独特作用;
GCG则通过增加能量消耗、促进脂肪分解进一步增强减重效果。
三靶点的协同激活,有望在降糖和减重两个维度上实现“1+1+1>3”的效应,同时兼顾对肝脏脂肪、血脂谱的改善。
目前,UBT251已获准在中国及/或美国开展成人2型糖尿病、超重/肥胖、慢性肾脏病、代谢相关脂肪性肝炎等多个适应症的临床试验,其适应症拓展潜力广阔。
03
II期临床数据详情
本研究是一项随机、双盲、安慰剂及司美格鲁肽对照的II期临床试验,共纳入211名中国2型糖尿病患者。患者基线平均糖化血红蛋白为8.12%,基线体重为80.1kg,基线BMI为29.1kg/m²。患者被随机分配接受每周一次的UBT251皮下注射(2mg、4mg、6mg剂量组)或安慰剂或司美格鲁肽1mg,连续给药24周。
降糖效果方面,治疗24周后,UBT251治疗组平均HbA1c降幅最高达2.16%,显著优于司美格鲁肽组的1.77%和安慰剂组的0.66%。这一降幅在数值上优于目前已上市的多款GLP-1类药物的历史数据,展现出强劲的血糖控制能力。
减重效果方面,UBT251治疗组平均体重降幅最高达9.8%,司美格鲁肽组下降4.8%,而安慰剂组仅下降1.4%。对于2型糖尿病患者而言,减重不仅有助于改善胰岛素抵抗,还能降低心血管风险,是综合获益的重要体现。
与安慰剂组相比,UBT251在腰围、血压和血脂等关键次要终点方面均显示出改善,提示其在心血管代谢风险综合管理中的潜在价值。
安全性方面,UBT251显示出良好的安全性和耐受性,与其他三激动剂临床试验中观察到的结果基本一致,未报告新的安全性信号。
04
赛道格局与未来市场潜力
GLP-1类药物的研发正经历从单靶点到双靶点、三靶点的快速迭代。目前,全球已上市的GLP-1类药物中,诺和诺德的司美格鲁肽(单靶点)和礼来的替尔泊肽(GIP/GLP-1双靶点)已占据主导地位。在更前沿的三靶点赛道,礼来的瑞他鲁肽(GLP-1/GIP/GCG)已进入III期临床阶段,并展现出超越双靶点的减重潜力。
UBT251作为国产首个进入III期临床的三靶点激动剂,其II期研究成功具有多重意义:一方面,验证了国产创新药在复杂多靶点药物设计上的研发能力;另一方面,与诺和诺德的BD合作为其全球开发铺平了道路。若后续III期临床顺利推进并获批上市,UBT251有望在降糖和减重两个百亿级市场中占据重要份额,成为联邦制药乃至中国创新药出海的又一重磅品种。
结 语
UBT251
II期研究的成功,是联邦制药在代谢疾病领域多年深耕的成果体现,也是中国创新药企在GLP-1这一全球热门赛道从“跟随”走向“并跑”的生动注脚。从降糖到减重,从单靶点到三靶点,UBT251用扎实的临床数据证明了自己的潜力。
随着III期研究的启动和全球商业化布局的推进,这款国产创新药有望早日惠及中国乃至全球的数亿代谢疾病患者。

