刚刚!科兴制药:「人干扰素α1b吸入溶液」拟纳入突破性治疗

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效

今日(3月24日),据CDE官网最新公示:科兴制药全资子公司深圳科兴药业有限公司自主研发的人干扰素α1b吸入溶液,拟被纳入突破性治疗品种名单,拟定适应症为小儿呼吸道合胞病毒性下呼吸道感染(肺炎、毛细支气管炎)。
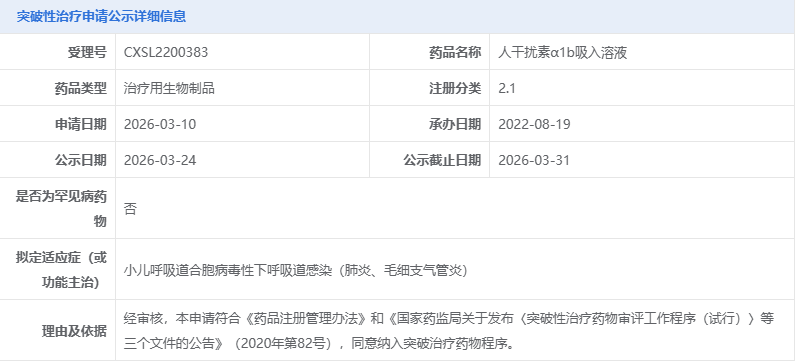
图片来源:CDE官网
呼吸道合胞病毒(RSV)是一种传染性极强的病毒,属于副黏病毒科肺炎病毒属,主要侵袭6个月以下的婴儿,引发细支气管炎和肺炎等下呼吸道感染,严重时可危及生命。对于较大儿童和成人,RSV通常仅导致类似感冒的上呼吸道症状,但其对婴幼儿的威胁却不容小觑。据统计,几乎所有儿童在2岁前都感染过呼吸道合胞病毒。我国因人口基数庞大,由RSV感染导致的儿童下呼吸道感染病例数在全球位居前列,相关临床治疗需求迫切。
作为儿童感染领域长期未被充分攻克的 “沉默杀手”,RSV 相关药物市场具备显著的发展潜力。据药智数据统计,2025年我国公立医院领域 RSV 相关产品销售额预计将超 4 亿元,市场扩容空间巨大。
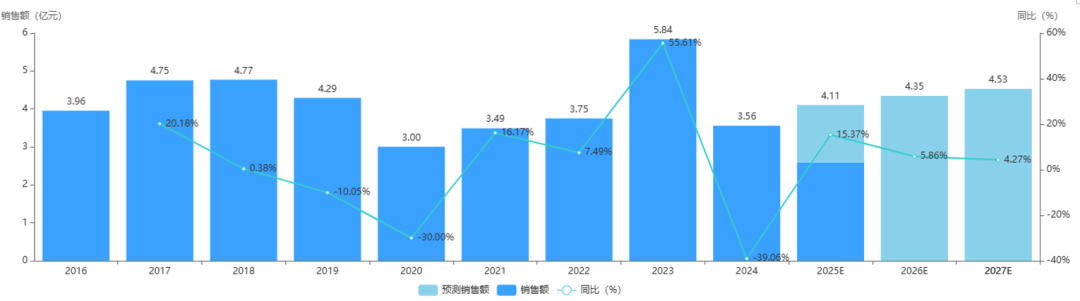
图片来源:药智数据-医院销售数据挖掘系统
干扰素(interferon,IFN)是一类具有广谱抗病毒、抗肿瘤和免疫调节作用的蛋白质,是机体天然免疫的关键组成部分。人干扰素α1b吸入溶液是科兴制药在抗病毒领域的又一大突破,干扰素α1b与细胞表面受体结合,激活抗病毒蛋白表达,抑制病毒复制,同时增强免疫细胞活性,帮助机体清除病毒。尤为关键的是,该药物为儿童专用药,采用雾化吸入的给药方式,有效成分可直达病灶,起效更迅速,且儿童患者的接受度和用药安全性更高。
从研发进程来看,科兴制药的人干扰素α1b吸入溶液推进节奏稳步提速:2022年11月获CDE批准临床;2024年3月完成III期临床试验首例受试者入组;2025年初斩获美国FDA临床试验批准,成为科兴制药中美双报的重要产品之一;2025年9月首次纳入突破性治疗名单,2今日再次获CDE公示拟纳入突破性治疗品种。
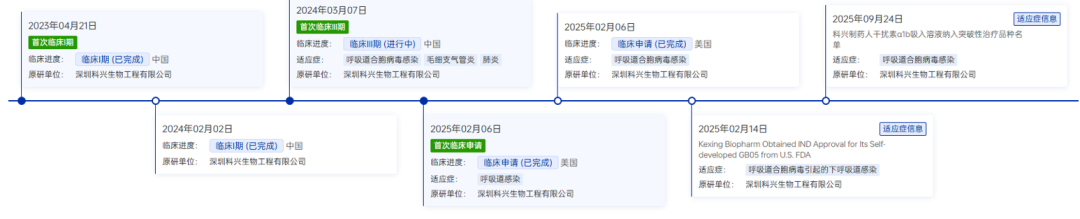
图片来源:药智数据-全球药物分析系统
此次人干扰素α1b吸入溶液拟纳入突破性治疗品种,意味着其在后续研发推进、审评审批环节将获得优先支持,药品上市进程将大幅加速。作为一款针对性解决婴幼儿RSV下呼吸道感染的儿童专用药,该产品的加速落地,将为国内婴幼儿 RSV 感染治疗提供全新选择,同时也将助力科兴制药进一步夯实抗病毒药物研发的核心竞争力,为全球儿童呼吸道健康保驾护航。


