恒瑞创新药吡咯替尼HER2阳性晚期乳腺癌长期随访数据更新亮相《英国医学杂志》 - 研发客,PharmaDJ

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效
2026年3月16日,由中国医学科学院肿瘤医院徐兵河院士牵头的恒瑞医药创新药吡咯替尼Ⅲ期PHILA研究的最新长期随访数据重磅发表于全球顶级医学期刊《英国医学杂志》(The BMJ)[1]。2023年,PHILA研究首次发表于《英国医学杂志》,以中位15.5个月的随访数据证实吡咯替尼联合曲妥珠单抗和多西他赛(PyroHT)方案一线治疗HER2阳性晚期乳腺癌患者具有显著的PFS获益和可控的安全性[2]。本次发表的长期随访数据,进一步确认了该方案的生存获益。
图1. PHILA研究再次登顶《The BMJ》
研究背景
曲妥珠单抗联合帕妥珠单抗的双靶方案是HER2阳性晚期乳腺癌的标准一线治疗。PHILA研究既往公布的结果证实[2,3],吡咯替尼联合曲妥珠单抗及多西他赛方案(PyroHT)一线治疗HER2阳性晚期乳腺癌患者具有显著的PFS获益和可控的安全性。2023年4月,国家药监局(NMPA)批准该方案用于治疗HER2阳性、晚期阶段未接受过抗HER2治疗的复发或转移性乳腺癌患者,这是吡咯替尼在乳腺癌领域获批的第三个适应症。
研究设计
PHILA研究为一项随机、双盲、多中心、安慰剂对照的Ⅲ期临床研究,共纳入590例未经系统治疗的HER2阳性转移性乳腺癌患者,患者按1:1随机分配至试验组(PyroHT,n=297)和对照组(HT,n=293),并根据既往(新)辅助曲妥珠单抗治疗(是 vs. 否)和激素受体状态(ER和/或PR阳性 vs. ER和PR阴性)进行分层。主要研究终点为研究者评估的PFS,次要研究终点包括PFS(独立评审委员会评估)、OS、客观缓解率(ORR)、肿瘤缓解持续时间(DoR)、临床获益率(CBR)和安全性。
研究结果
截至2024年4月30日的随访数据
数据截止时间为2024年4月30日[2],PyroHT组与HT组的中位随访时间分别为35.7和34.3个月。
mPFS最终分析:PyroHT组和HT组研究者评估的中位PFS分别为22.1 vs. 10.5个月(HR=0.44,95% CI:0.36-0.53;P<0.0001)。与HT组相比,PyroHT组的研究者评估的PFS在最终分析中维持了获益,所有预设的亚组均显示出一致的PFS获益。
mOS分析:与HT组相比,PyroHT组的OS更具优势(HR=0.64,95% CI:0.46-0.89;单侧名义P=0.004)。两组的中位OS均未达到。
截至2025年5月30日的随访数据
长期随访数据显示,截止时间为2025年5月30日[4],PyroHT组与HT组的中位随访时间分别为46.5和44.6个月。PyroHT组中仍有75例患者(25.3%)在接受研究治疗,而HT组仅为19例(6.5%)在接受研究治疗。
mPFS分析:与既往结果一致,PyroHT组患者获得了持久的PFS(研究者评估)获益(HR=0.44,95% CI:0.36-0.54;单侧名义P<0.0001)。PyroHT组和HT组的3年、4年、5年PFS率分别为40.4% vs. 9.7%,31.9% vs. 7.6%,29.2% vs. 4.3%(图2)。所有亚组均显示出一致的PFS获益。
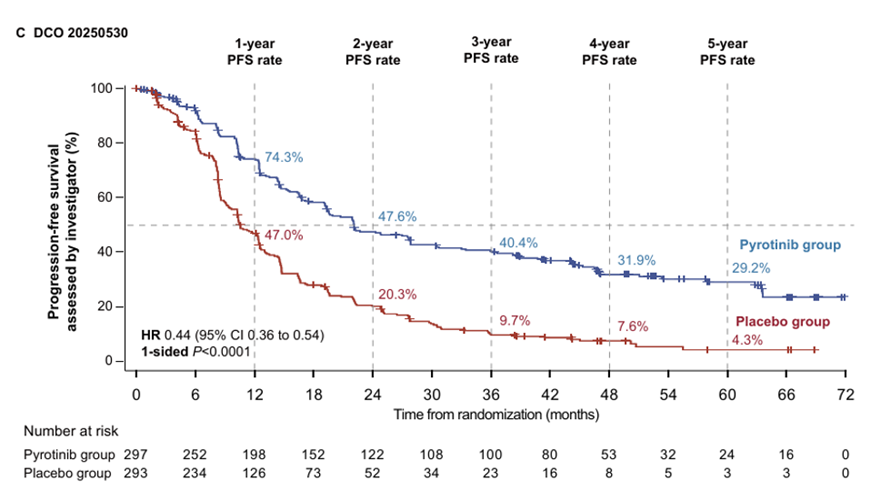
图2. 研究者评估的PFS分析(cut off:2025.05.30)
PFS亚组分析:对于既往接受过(新)辅助曲妥珠单抗治疗的患者,PyroHT组(n=46)的中位PFS为62.8个月(95% CI:19.2-无法评估),而HT组(n=42)为10.4个月(95% CI:6.4-13.2)(图3)。
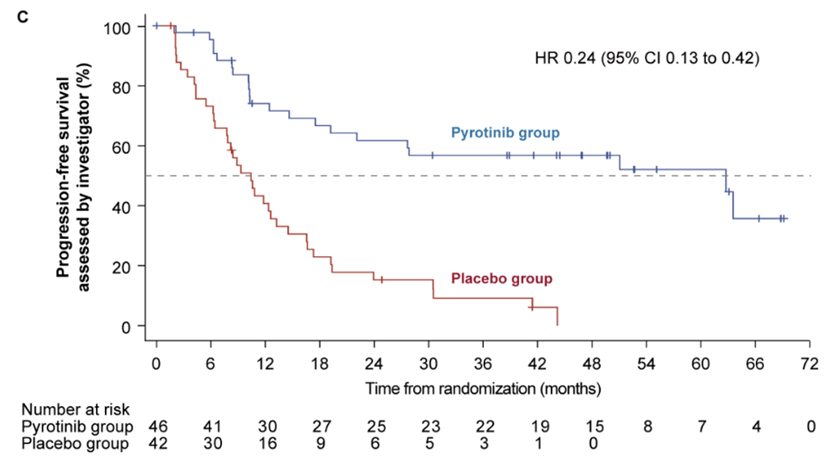
图3. 既往接受过(新)辅助曲妥珠单抗治疗的患者的PFS
mOS分析:与HT组相比,PyroHT组的OS更具优势(HR=0.74,95% CI:0.56-0.98;单侧名义P=0.02)。两组的中位OS均未达到(图4)。
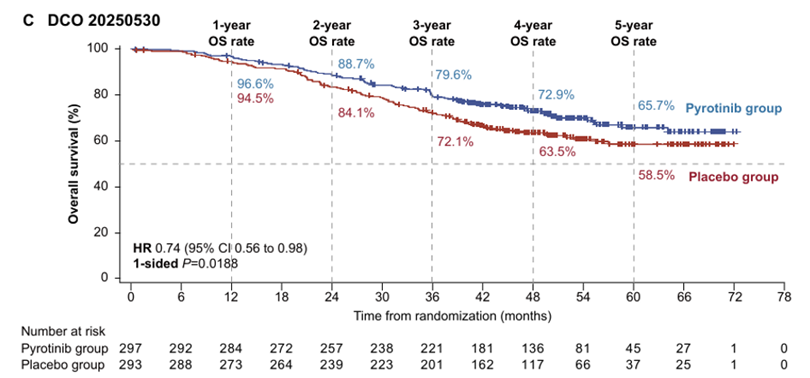
图4. OS分析(cut off:2025.05.30)
ORR分析:PyroHT组与HT组的ORR分别为84.2%(250/297,95% CI:79.5-88.1)和71.7%(210/293,95% CI:66.1-76.8)。
CBR分析:PyroHT组与HT组的CBR分别为88.6%(263/297,95%CI:84.4-91.9)和80.9%(237/293,95% CI:75.9-85.2)。
DoR分析:PyroHT组为22.3个月(95% CI:17.9-29.3),HT组为10.4个月(95% CI:8.4-12.4)。
安全性
安全性数据截止日期为2024年4月30日。其安全性与既往中期分析一致,未发现新的安全信号。
小结
PHILA研究的PFS最终分析证实,相较于HT方案,PyroHT方案用于HER2阳性转移性乳腺癌一线治疗,显著延长了mPFS(22.1个月 vs. 10.5个月,HR=0.44),降低了36%的死亡风险(HR=0.64),其5年生存率达66%、无进展生存率达30%。在长期随访45.5个月后,疗效持续稳定,各预设亚组均显示出一致的获益,其中既往接受(新)辅助曲妥珠单抗的患者mPFS达62.8个月,且能延缓至脑转移发生时间(中位16.6个月 vs. 9.1个月)。
安全性与既往中期分析一致,未发现新的安全信号,整体安全性可控。
参考文献:
[1] Xu BH, Ma F, Yan M, et al. BMJ 2026;392: e087259.
[2] Xu BH, Yan M, Ma F, et al. BMJ 2023; 383: e076065.
[3] Xu BH, Yan M, Ma F, et al. 2024 SABCS. GS1-03.
[4] Xu BH, Ma F, Yan M, et al. 2025 SABCS. PS5-01-02.

