Science论文揭示超快速硼偶联技术开启蛋白质疗法“定制化”新纪元

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效
来自苏黎世联邦理工学院(ETH)的化学家找到了一种通过"封装"一种独特反应性硼化合物来生产难溶蛋白质的方法。这种方法为定制蛋白质疗法的合成开辟了新的可能性,包括癌症治疗。
许多对现代医学和科学至关重要的蛋白质都是难溶的。这其中就包括众多的信号蛋白和蛋白激素,以及所有锚定在细胞膜上的受体——目前约60%的药物有效成分都以这些受体为靶点。如果这些蛋白质的浓度超过某个阈值,它们就会聚集在一起并失去功能。
这种聚集使得在实验室中无法通过化学合成方式生产这些分子。由于专门的合成机器人生产蛋白质总是需要将多个片段连接成一个完整的蛋白质,通常只要有一个难溶的蛋白质片段就足以阻碍生产。这是因为化学家们目前用来连接蛋白质片段的方法,只有在这些片段以相对较高的浓度存在于溶液中时才能起作用。

由苏黎世联邦理工学院有机化学实验室教授 Jeffrey Bode 领导的研究人员现已找到一种方法,即使是难溶的蛋白质片段也能连接成有功能的蛋白质。为此,他们利用了一种含硼元素的化合物的特殊性质。这些发现发表在《科学》杂志上。
缓慢的碳化学带来的浓度限制
ETH 方法与常规方法的最大区别在于偶联反应的速度。虽然在生物体的细胞中,得益于酶的作用,生物化学反应发生得非常快,但这类反应在实验室中通常必须在非自然的高浓度下进行。这是因为反应发生得越慢,反应物的浓度就必须越高,才能按计划进行。
Bode 团队开发的新偶联方法速度快了约 1000 倍,因此也适用于比之前低 1000 倍的浓度。
硼为新的化学可能性铺平道路
ETH 化学家通过将硼原子引入碳基分子中,从而加速了反应。这些原子不存在于天然分子中。
就其许多性质而言,类金属硼的行为方式颇为不同。当它与金属键合时,会产生极其坚硬且耐热的金属合金。另一方面,它可以在实验室中与非金属碳、氧或氮键合,产生通常具有不寻常反应性质的分子。2010年,日本研究者 Suzuki Akira 和美国研究者 Richard Heck 因开发用于实验室合成天然物质的基于硼的偶联反应而获得诺贝尔化学奖。
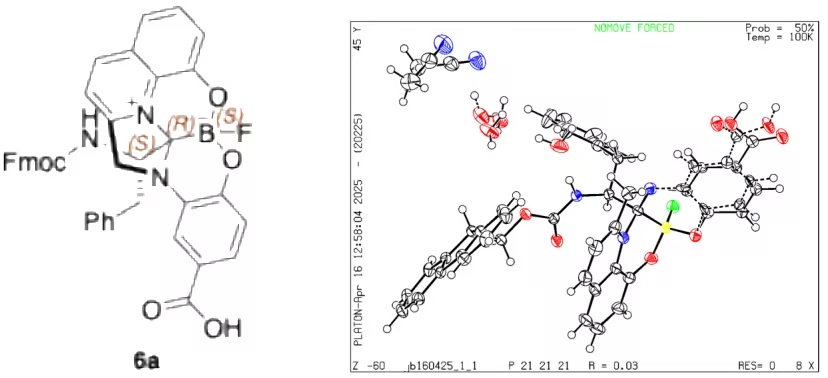
Bode 解释说:"对于纯碳基系统,我们触及了反应速率的基本极限。通过扩展到以前未探索的硼基试剂,我们进入了一个领域,即使是连接大生物分子的挑战性反应也能极其迅速地发生。"
保护其免受强酸的崎岖之路
2012年,Bode 的研究小组首次证明,一种将硼与氟结合形成新化学基团的碳化合物可以极其快速、可靠地连接蛋白质片段。然而,这种化合物在强酸存在下不稳定,因此无法用于自动化合成。
为了让这种敏感的硼化合物能够承受标准实验室机器人中使用的严酷条件,它需要化学"包装"的保护——但这说起来容易做起来难。研究人员测试了四年的各种策略,基本没有成功。突破最终是偶然发生的,当时一名博士生测试了一种团队原以为行不通的方法。由此产生的保护性化合物从三个侧面"抓住"硼基团,使其在蛋白质生产过程中不会被酸分解。
Bode 说:"这种基础研究,我们可以冒险进入未知的科学领域而不保证成功,只有得益于瑞士国家科学
基金
会和 ETH 的无限制资金才成为可能。"
非天然氨基酸与癌症疗法
ETH 的方法意味着现在可以使用标准实验室技术生产新的肽和蛋白质药物,或易聚集的、具有医学重要性的膜蛋白。
此外,具有特殊性质的非天然氨基酸也可以在难溶蛋白质上的任何所需位置引入。例如,如果化学家想在特定位置将蛋白质与活性物质连接起来,他们可以有目的地将这些构建模块整合到蛋白质中。
在其他应用中,通过这种方式创建的抗体-药物偶联物被用于不伤害健康组织的癌症疗法。
目前尚不清楚该方法将如何在临床实践中使用。2020年,Bode 共同创立了 ETH 衍生公司 Bright Peak Therapeutics,该公司利用其研究小组开发的技术来开发抗癌
免疫
疗法。
一种初始治疗剂已经在进行临床试验,新的基于硼的方法可能有助于进一步扩展该衍生公司的产品线。(
生物谷
Bioon.com)
参考文献:
Philipp E. Schilling et al,
Zwitterionic organoboron complexes for overcoming the concentration barrier in chemical protein synthesis
, Science (2026). DOI: 10.1126/science.aea7511.

