颠覆传统认知!《Nature》阐明miRNA降解的“双因子认证”机制:触发RNA改变AGO结构,被E3连接酶特异性识别并泛素化

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效
MicroRNAs(miRNA)与Argonaute(AGO)蛋白结合,形成复合物,从而下调目标 RNA,包括大多数人类基因的信使 RNA。在每个复合物中,miRNA 与目标 RNA 相互结合,而Argonaute则发挥效应功能,同时还能保护 miRNA 免受细胞核酸酶的破坏。尽管关于 miRNA 直接调控基因的知识已相当丰富,但对于 miRNA 本身是如何被调控的却知之甚少。
有一种调控 miRNA 的途径涉及被称为“触发(trigger)”RNA 的不寻常靶标,它们打破了常规的调控逻辑,反而下调 miRNA。这种靶向 miRNA 的降解(TDMD)被认为需要一种称为“cullin–RING E3 连接酶”的途径,因为它依赖于cullin CUL3 以及其他泛素化组件,包括 BC-box蛋白 ZSWIM8。ZSWIM8 对小鼠围产期存活和大多数短寿命 miRNA 的不稳定化是必需的,这表明 TDMD 具有生物学重要性。

2026年3月18日,麻省理工学院David P. Bartel团队在
Nature
在线发表题为
“The E3 ubiquitin ligase mechanism specifying targeted microRNA degradation”
的研究论文,该研究通过生物化学和细胞实验证实了 ZSWIM8 - CUL3 E3 连接酶通过与 AGO 结合并进行多聚泛素化这一过程是 TDMD 的关键调控步骤,从而定义了一个独特的 Cullin - RING E3 连接酶类别。
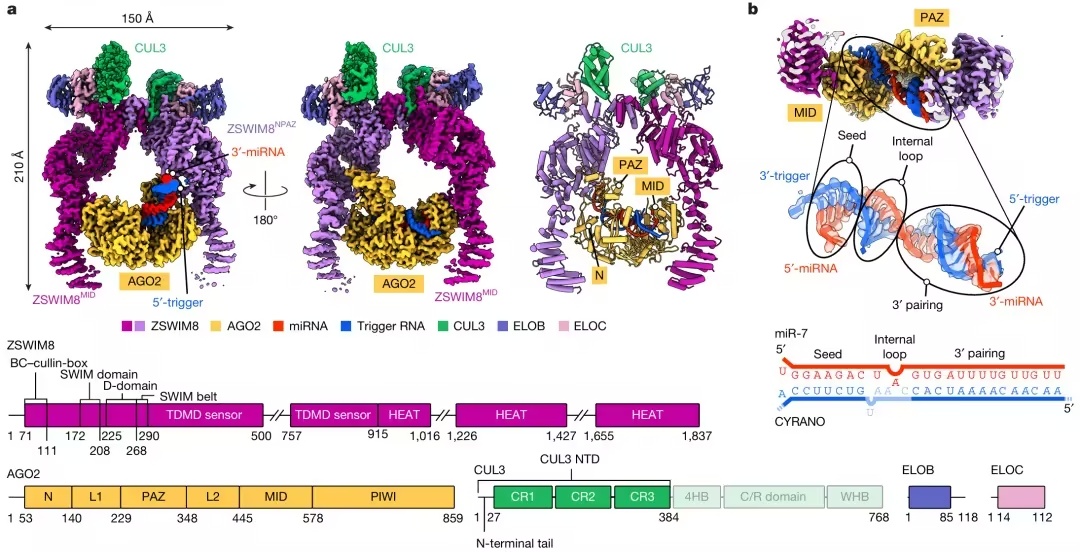
ZSWIM8 蛋白会围绕着 AGO2–miR-7–CYRANO 复合物形成一个二聚体结构(图源自
Nature
)
冷冻电子显微镜分析表明,ZSWIM8 能识别由 miRNA 与触发物配对所形成的独特的 AGO 和 RNA 构象。通过普遍适用的 RNA-RNA、RNA-蛋白质和蛋白质-蛋白质相互作用,确立了 AGO 蛋白质泛素化特异性。E3 连接酶所识别的底物特征不符合传统的降解信号序列,而是建立了用于指定蛋白质泛素化底物的两个 RNA 因子认证机制。
参考消息:https://www.nature.com/articles/s41586-026-10232-0

