Cell:超越ATP!线粒体通过“PEP穿梭”调控脂肪生成,为治疗脂肪肝和糖尿病提供全新靶点

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效
线粒体除了提供三磷酸腺苷(ATP)外,还会提供多种代谢物以满足细胞特定的需求。其中一种代谢物是磷酸烯醇式丙酮酸(PEP),它比 ATP 具有更高的能量磷酸键,并且具有多种生物学功能。然而,线粒体产生的 PEP 如何被输送到细胞质并满足细胞特定需求仍不清楚。
2026年3月17日,哈佛医学院Shingo Kajimura团队在
Cell
在线发表题为
“Mitochondrial control of glycerolipid synthesis by a PEP shuttle”
的研究论文,该研究表明,SLC25A35 调节线粒体 PEP 外流和甘油生成,在利用丙酮酸到 PEP 跳跃途径的脂肪生成细胞中发挥作用。重构和结构研究表明,SLC25A35 以 pH 梯度依赖的方式运输 PEP。
在脂肪细胞中,SLC25A35 的缺失会阻碍线粒体 PEP 转化为甘油-3-磷酸,从而减少甘油脂质的合成。值得注意的是,对肥胖小鼠肝脏中 SLC25A35 的抑制减轻了脂肪变性和改善了全身葡萄糖稳态。总之,这些结果表明,线粒体通过 SLC25A35 提供 PEP 来促进甘油脂质的合成,将具有脂肪生成功能的线粒体作为限制甘油脂质合成的目标,这是肝脂肪变性和 2 型
糖尿病
发病过程中的关键步骤。

线粒体作为代谢枢纽,能够为细胞内的各个亚细胞区域(包括细胞核、内质网和脂滴)提供 ATP 以及必要的代谢物质。与线粒体活动密切相关的一个例子就是磷酸烯醇式丙酮酸(PEP)。PEP 拥有细胞内最高的能量磷酸键,其水解为丙酮酸和无机磷酸时的标准吉布斯自由能变化(ΔG°′)约为−61.9 kJ mol−1,这一数值远高于 ATP 转化为 ADP 的−30.5 kJ mol−1。如此巨大的负 ΔG°′使得 PEP 在各种代谢过程中成为一种多功能的能量供体。
在糖酵解过程中,它通过丙酮酸激酶驱动 ATP 的生成;在糖异生过程中,PEP 是肝脏中必不可少的底物;而在甘油生成过程中,PEP 被转化为甘油-3-磷酸(G3P),这是脂肪酸酯化为甘油脂(包括脂肪组织和肝脏中的甘油三酯和磷脂)所必需的甘油骨架。此外,PEP 还参与胰腺β细胞中 ATP 依赖性胰岛素分泌以及活化 T 细胞中 Ca²⁺信号的调节。这种能量含量极高的分子是如何生成、传递,并满足细胞类型特定需求的,目前仍是个谜。
为了从丙酮酸中生成这种富含高能量的磷酸烯醇式丙酮酸(PEP),细胞必须通过两步反应来克服能量障碍:第一步是一个消耗 ATP 的反应,通过丙酮酸羧化酶(PCX)将丙酮酸转化为草酰乙酸(OAA);第二步是一个消耗三磷酸鸟苷(GTP)的反应,通过磷酸烯醇式丙酮酸羧基激酶(PEPCK)将 OAA 转化为 PEP。值得注意的是,PEP 可以通过丙酮酸羧基激酶(C-PEPCK 或 PCK1)在细胞质中由 OAA 合成,也可以通过丙酮酸羧基酶 2(也称为 M-PEPCK)在线粒体中由 OAA 合成。
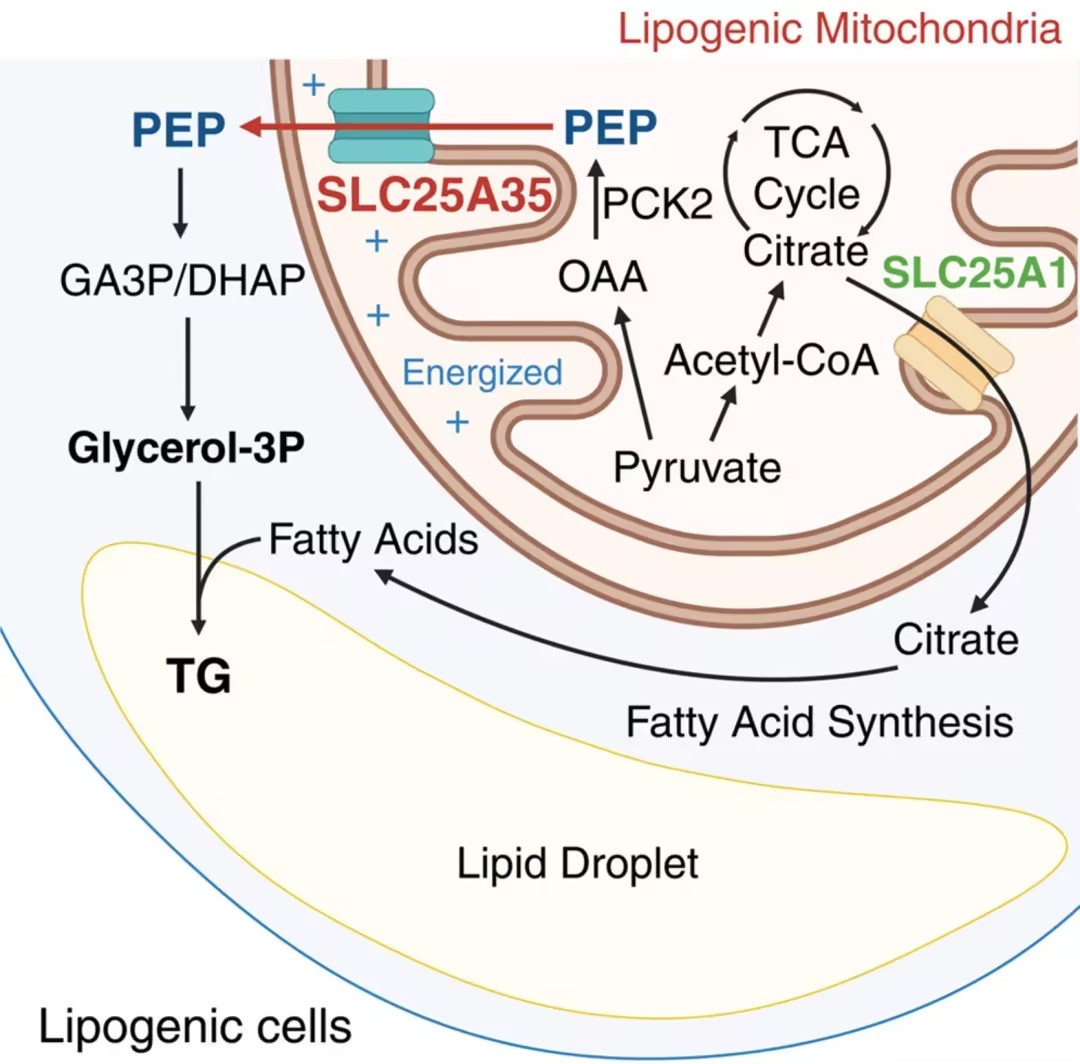
文章模式图(图源自
Cell
)
长期以来,人们在糖异生过程中对 PCK1 给予了较多关注,原因在于:(1)在啮齿动物肝脏中,PCK1 的含量高于 PCK2(注意:人类的 PCK2 约占 50%);(2)PCK1 的表达和活性受到
营养
和激素信号的动态调节,包括禁食;(3)肝脏中 PCK1 的过表达会导致
高血糖
;(4)抑制 PCK1 可减弱由乳酸/丙酮酸引起的肝脏糖异生,尽管肝脏特异性 Pck1 基因敲除(KO)小鼠由于代偿性的肾脏糖异生而能保持血糖正常。因此,可以合理地认为,PEP 主要是在细胞质中生成的。
该研究表明,SLC25A35 调节线粒体 PEP 外流和甘油生成,在利用丙酮酸到 PEP 跳跃途径的脂肪生成细胞中发挥作用。重构和结构研究表明,SLC25A35 以 pH 梯度依赖的方式运输 PEP。在脂肪细胞中,SLC25A35 的缺失会阻碍线粒体 PEP 转化为甘油-3-磷酸,从而减少甘油脂质的合成。值得注意的是,对肥胖小鼠肝脏中 SLC25A35 的抑制减轻了脂肪变性和改善了全身葡萄糖稳态。总之,这些结果表明,线粒体通过 SLC25A35 提供 PEP 来促进甘油脂质的合成,将具有脂肪生成功能的线粒体作为限制甘油脂质合成的目标,这是肝脂肪变性和 2 型糖尿病发病过程中的关键步骤。
参考消息:https://www.cell.com/cell/abstract/S0092-8674(26)00224-2

