【认知生理】BPSD产生机制的再诠释:基于小脑行为调谐系统

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效
[ 摘要] BPSD(behavioral and psychological symptoms of dementia)长期被视为认知症过程中的附属性精神行为问题,但这一理解难以解释其高发生率、强异质性及与环境、照护方式和任务结构的高度耦合。与此同时,现代神经科学已明确,小脑并非仅服务于运动协调,还深度参与预测加工、时间组织、认知自动化、语言调节与社会认知;小脑认知-情感综合征(CCAS)的相关研究进一步表明,小脑损害可稳定地产生执行、语言、情感和行为调节异常。基于此,本文提出:BPSD可被重新理解为“小脑所参与的行为调谐系统(Cerebellar Behavioral Tuning System, CBTS)”失稳后的综合临床表型。该系统通过预测性预调、时序排序、误差校正、自动化编译与社会情境适配,维持行为输出的准、顺、稳。进一步地,最新研究显示,传统上与卵母细胞透明带相关的核心结构蛋白 ZP2,在人类小脑颗粒细胞中被重新利用,并由脑桥苔状纤维输入诱导,参与球状突触发育及神经活动调节。这提示,小脑行为调谐功能的系统级失稳之下,可能还存在一个更微观的连接调谐层。本文据此提出:ZP2或可被视为维持CBTS微连接精度与低噪声状态的候选分子支架之一。该框架并不否定额叶、边缘系统和海马的重要性,而是强调小脑及其相关微回路调控机制在BPSD形成中的上游参与意义,并为分层评估和非药物干预设计提供新的理论基础。
关键词 BPSD;小脑;行为调谐系统;CBTS;ZP2;CCAS;预测加工;时间组织;社会认知;非药物干预
一、问题提出:BPSD为何需要新的神经框架
BPSD包括冷漠、焦虑、抑郁、激越、攻击、妄想、幻觉、睡眠障碍、食欲异常与异常运动行为等,贯穿多数认知症患者的病程;综述指出,痴呆患者在病程中出现某种形式BPSD的比例可高达约90%,且这些症状显著增加照护负担、住院风险与医疗成本。传统解释常把BPSD分拆为情绪问题、精神病性症状或额叶行为异常,但这种分割式视角难以说明:为何同一患者会在任务复杂、环境变化、照护压力和社交误解时出现一整串跨情绪、跨行为、跨社交维度的症状。
另一条正在成熟的证据链来自小脑研究。近二十余年,小脑已被重新定义为不仅参与运动协调,而且参与执行功能、语言、情感调节、时间加工与社会认知。CCAS(小脑认知-情感综合征)及其后续量表和综述显示,小脑损害可以引起执行障碍、语言异常、视觉空间缺陷和情感调节失衡,这说明小脑本身就是认知与行为调谐系统的重要节点,而非纯粹的运动附属结构。
基于这两类进展,本文提出:BPSD可被重新理解为“小脑所参与的行为调谐系统(Cerebellar Behavioral Tuning System, CBTS)(Figure 1)”失稳的临床表型之一。 这里所谓“行为调谐”,并非产生行为内容本身,而是让行为在时间上有序、在强度上适中、在社会情境中合宜、在执行中低噪声。
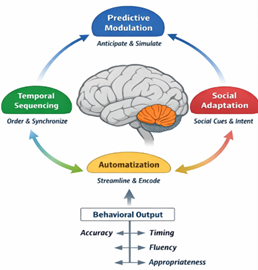 Figure 1 CBTS框架图
Figure 1 CBTS框架图
二、小脑的功能扩展:从运动协调到行为调谐
小脑最经典的作用是运动协调。它通过误差校正、节律调控和动作平滑化,使动作输出更精准、更连贯、更低噪声。若将这一原则抽象出来,小脑本质上并不是“只管运动”,而是在做一件更一般的事情:把复杂输出调成“准、顺、稳”。这一点恰恰解释了为什么小脑也会被招募进认知和情感系统。
现代多领域综合研究表明,小脑参与预测加工、时间顺序编码、认知流程自动化、语言输出调节与社会认知中的意图理解和互动预测。换言之,小脑不仅校正肢体动作,也校正“认知动作”“语言动作”和“社会动作”。当个体需要完成穿衣、洗澡、对话、回应照护、理解场合规则或预判他人意图时,小脑都可能通过与额叶、边缘系统及联想皮层的回路协作,充当后台调谐器。
因此,与其把小脑简单称为“运动器官”,不如把它理解为行为调谐器。这个调谐器的任务包括:第一,预测下一步会发生什么;第二,把连续动作或步骤排成合适的时间序列;第三,将高耗能的控制流程逐步自动化;第四,根据社交对象和情境修正反应方式。只要这些层面任一失稳,临床上就可能出现并非局限于运动、而是跨越情绪、行为和社会功能的异常表现。
三、BPSD症状谱与CBTS失稳的对应关系
若以CBTS为框架审视BPSD,可以发现许多症状并非彼此孤立,而是共同指向“行为调谐失败”(Figure 2)。
首先, 焦虑、易激惹、灾难化反应与照护抗拒,可被理解为预测系统失稳。当患者无法稳定预测外界刺激、照护动作、任务步骤或他人意图时,环境便显得突然、不可控且高威胁,于是最常见的防御性输出就是退缩、抗拒、愤怒或攻击。这与BPSD中常见的激越、紧张、不安和被害样反应高度吻合。
其次 ,重复提问、重复动作、游走、傍晚症状加重及多步骤任务中的突然爆发,可被理解为时间组织和序列整合失败。小脑擅长对短时间尺度上的节律、顺序和切换进行精细调节;一旦这一层粗糙化,患者在洗澡、更衣、如厕、进食等多步骤活动中就容易丢失节奏,形成“做不下去—烦躁—拒绝”的链条。很多被贴上“行为问题”标签的表现,实质上可能是任务时序超过了患者当前的调谐容量。
再次, 冷漠、启动困难、目标维持差和‘不配合’,可被理解为认知自动化失灵。对于健康个体,大量日常行为是在低耗能、半自动化的状态下完成的;但当小脑-皮层自动化回路失效,原本熟练的行为也会变得高负荷、高失败率。患者于是表现为拖延、回避、疲惫、表面冷漠,甚至在照护场景中被误认为“故意不合作”。实际上,这更像是行为程序无法被顺利编译和调用。
最后, 脱抑制、社交误解、被害感、妄想样解释和不合宜行为,可被理解为社会认知调谐障碍。小脑被证实参与社会序列理解、他人意图预测和行为生成调控;一旦这一网络失稳,患者就更难正确解读照护者的表情、语气和动作意图,也更难按场合调整自己的语言与行为。许多所谓“精神行为症状”,本质上可能是社会预测失败后的防御性或错配性输出。
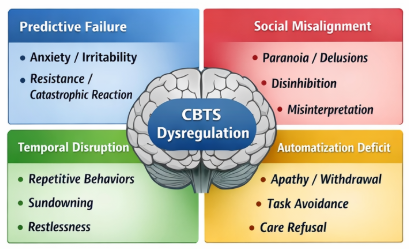 Figure 2 BPSD症状映射图
Figure 2 BPSD症状映射图
四、BPSD重构:从 “ 症状标签 ” 到 “ 网络失稳表型 ”
将BPSD放入CBTS框架,最大的理论收益在于:它不再只是零散症状的堆积,而成为一个具有层级结构的网络表型。传统分类倾向于把妄想归精神病性、把激越归行为性、把冷漠归情感性、把游走归运动性;但临床现实中,这些症状往往缠绕出现,并受环境噪声、照护方式、任务复杂度和社交压力显著影响。CBTS模型则指出,这种“缠绕性”恰恰来自它们共享了一个更上游的失稳层:行为调谐后台。
这一框架并不否认额叶、边缘系统、海马或默认网络的重要性。相反,它提供了一个更合理的分层:海马和内侧颞叶更偏向记忆编码与病理脆弱层,额叶更偏向计划与抑制控制层,而小脑则更像是把这些输出“调顺、调稳、调合宜”的后台结构。2024年的综述指出,小脑在神经退行性疾病中并非旁观者,AD小脑可见Aβ/Tau相关改变,并与认知和行为变化相关;此外,一些研究提示小脑可能在早期具有代偿意义。
因此,BPSD的形成可以被理解为:在神经退行过程中,记忆、执行、情感与知觉系统逐步受损,而小脑-皮层行为调谐系统无法再对这些受损输出进行有效滤波、排序和社会适配,于是症状从“脑内失衡”变成“行为外显”。这使得BPSD更接近一种网络动力学失稳的临床窗口,而不是单纯的附属症状。
五、照护与干预启示:重建可预测、可排序、可参与的世界
若BPSD部分源自CBTS失稳,那么干预重点就不应只放在“压制异常行为”,而应转向帮助患者恢复最基本的行为调谐条件。当前系统综述和指南普遍建议,BPSD的一线管理应优先采用非药物干预,包括优化物理与社会环境、照护者培训、个体化活动和结构化支持;药物治疗多用于风险高或症状重的场景。
从CBTS视角看,这些建议之所以有效,并不只是“安慰患者”,而是在降低预测负荷、减少时序混乱和稳定社会信号。具体而言:简化任务步骤、固定活动节律、减少突发刺激、用更稳定的语气和动作接近患者、把多步骤任务拆成可完成的小单元、提供重复而低威胁的引导,这些做法都可以理解为在外部帮助患者完成“行为调谐”。换言之,良好照护不是单纯管理症状,而是替代性地为患者搭建一个其仍能预测、排序和参与的环境系统。
这一思路也有助于重新理解“照护抗拒”。很多时候,患者并不是主观上拒绝合作,而是因为任务太快、步骤太多、身体姿势不稳、语言指令过载或社交信号令人紧张,导致CBTS无法维持足够的预测和排序能力,于是只能以僵住、退缩、挣扎或发怒作为输出。这一解释比单纯将其视为“精神症状发作”更接近临床现场。
六、ZP2核心结构蛋白的功效及其对小脑的影响
2026年3月,耶鲁大学医学院Nenad Sestan教授领导的研究团队在《Cell》期刊上发表了一项突破性研究,一个传统上被认为只在卵子表面发挥作用的“精子受体”蛋白——ZP2,竟然在人类小脑的颗粒神经元中被“二次利用”,精细地调控着突触的发育与功能。本文将基于这项研究的原文数据,从专家的视角,深入、准确地解析这一发现的全貌及其深远意义。ZP2 这一传统上被视为卵母细胞透明带核心结构蛋白、参与精卵识别的分子,在人类成年小脑中发生了出人意料的“二次利用”。研究团队在跨物种成年灵长类小脑皮层的单核转录组和染色质可及性图谱中发现,ZP2及其潜在互作分子在人类小脑颗粒细胞中富集,并构成人类小脑特异性分子特征的一部分。更关键的是,实验结果提示 ZP2 表达可由脑桥苔状纤维输入诱导,且与小脑球状突触相关突触蛋白下降和神经元电生理活动降低相关。由此可见,ZP2在小脑中的作用并非简单的结构性存在,而更可能是一个参与突触组织、连接筛选和神经活动调谐的调控分子。
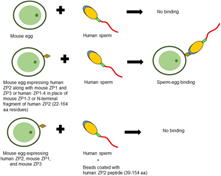 Figure 3 ZP2主导的生殖系统单精受精
Figure 3 ZP2主导的生殖系统单精受精
这一发现对本文提出的CBTS框架具有重要补充意义。若说CBTS描述的是小脑在预测、时序组织、认知自动化、语言调节和社会认知中的系统级功能角色,那么ZP2则提示:这些高阶功能并非凭空产生,而可能依赖于更微观的连接约束与突触精度机制。从当前证据看,ZP2并不像传统突触促进分子那样单纯增加连接数量,而更像一个限制性调节器:它可能通过抑制过强或过多的球状突触形成,降低局部神经活动强度,从而帮助小脑维持更合适的输入配额、更低的网络噪声和更高的时间精度。换言之,ZP2的潜在功效,不在于“让小脑更兴奋”,而在于让小脑更精细、更有边界、更可调谐。
这一点尤其契合小脑在人类脑进化中的位置。Human Protein Atlas 显示,ZP2 在脑内的突出信号位点是小脑突触,而不是海马等经典记忆结构;其脑区汇总页面把 ZP2 的脑内高置信特征主要指向小脑相关突触表达,且海马形成区总体表达极低。这个事实提示,ZP2在脑内并非普遍表达分子,而更像一个与小脑特异性微回路组织相关的候选分子。
从功能上推断,ZP2可能为小脑提供三方面支持。 其一 ,是输入筛选:在人类小脑接收来自脑桥的大量皮层整合信息时,ZP2可能帮助颗粒细胞层限制不恰当或过量的突触接入,使输入保持可分辨、可排序。 其二 ,是连接唯一性或配额控制:它可能并不允许任意增加突触,而是帮助小脑将连接维持在一个适合预测计算和误差校正的范围内。其三,是活动调谐:通过降低部分神经元电生理活动和突触蛋白水平,ZP2可能在局部网络中发挥“降噪”和“稳定器”作用。需要强调的是,这些推断与现有实验结果方向一致,但其与具体认知功能、老化进程及BPSD之间的因果链,目前仍需后续研究验证。
将ZP2纳入BPSD讨论的意义,在于它为“小脑行为调谐系统失稳”提供了一个可能的分子层接口。本文前文已论证,BPSD中的焦虑、激越、重复行为、冷漠、照护抗拒、社交误解与脱抑制,可被理解为小脑参与的预测、时序、自动化和社会认知调谐失败后的外显。若ZP2确实参与维持小脑微连接层的精度与活动边界,那么它就可能不是直接决定某一BPSD症状的“单一病因分子”,而更像是维持CBTS正常运行的底层分子支架之一。在这一意义上,ZP2的重要性不在于解释全部BPSD,而在于提示我们:BPSD的形成,除了额叶、边缘系统和神经递质失衡之外,还可能涉及小脑微回路连接规则的失准。
当然,当前证据也有明确边界。现有直接功能数据主要集中于人类小脑颗粒细胞与球状突触,尚未证明ZP2在BPSD患者中的表达改变,也未证明其变化可直接预测MBI、MCI或AD相关行为症状。其次,公开数据库提示 ZP2 在脑内具有明显的小脑偏向性,而非海马主导表达,因此它更适合作为“网络调谐层分子”来理解,而不是作为解释AD或PD经典海马病理沉积的主分子。换言之,ZP2最可能指向的是网络精度的上游维护问题,而不是病理蛋白沉积本身。
因此,若从理论上整合本文观点,可以提出一个更完整的链条:在人类进化中,小脑被更深地纳入预测、时序、计划和社会认知回路;与此相适应,小脑发展出更严格的微连接调谐机制,其中可能包括ZP2这样的“再利用分子”;当老化、疾病或长期低质量使用导致这一微连接调谐层失稳时,CBTS的系统级功能便随之下降,进而表现为BPSD中的多样化行为与心理症状。这个模型尚待验证,但它为BPSD研究提供了一个从分子—微回路—网络—症状逐层贯通的新视角。
七、结论
BPSD不应再被简单理解为认知症过程中的附属性精神行为问题。随着小脑功能观的扩展,更合理的理解是:小脑所参与的行为调谐系统,通过预测、时间组织、认知自动化、语言调节与社会认知,维持行为输出的准、顺、稳;当这一系统在网络层面失稳时,临床上便可出现焦虑、激越、重复行为、冷漠、照护抗拒、社交误解和脱抑制等BPSD谱系表现。与此同时,最新的ZP2研究进一步提示,这种系统级失稳之下,可能还存在一个更微观的连接调谐层:ZP2作为在人类小脑颗粒细胞中被重新利用的分子,可能通过调节球状突触形成与神经活动边界,帮助维持小脑微回路的精度、配额与低噪声状态。虽然目前尚无证据证明ZP2可直接解释BPSD,但它为“小脑行为调谐系统失稳”提供了重要的分子线索。由此,BPSD可以被重新定位为一种横跨微连接失准、网络失稳与行为外显的复合临床表型;这一框架不仅有助于深化病理机制理解,也为未来的分层评估和非药物干预设计提供了更具生物学层次感的理论基础。
杨金宇 第一稿(健康界) 2026.3.19
参考资料
[1] Cerejeira J, et al. Behavioral and Psychological Symptoms of Dementia. Front Neurol. 2012.
[2] Scassellati C, et al. Behavioral and Psychological Symptoms of Dementia. Int J Mol Sci. 2020.
[3] Anantapong K, et al. Behavioural and psychological symptoms of people living with dementia. 2025.
[4] Argyropoulos GPD, et al. The Cerebellar Cognitive Affective/Schmahmann Syndrome. Brain. 2019.
[5] Hoche F, et al. The cerebellar cognitive affective syndrome scale. Brain. 2017.
[6] Ahmadian N, et al. The Cerebellar Cognitive Affective Syndrome—a Meta-analysis. 2019.
[7] Reumers SFI, et al. Cognition in cerebellar disorders. 2025.
[8] Thieme A, et al. Optimizing selectivity of the CCAS scale / social cognition relies on the cerebellum. 2025.
[9] Liu G, et al. Cerebellum in neurodegenerative diseases. 2024.
[10] Jesto S, et al. Nonpharmacological nursing interventions for BPSD. 2024.
[11]Byeon G, et al. Clinical Practice Guidelines for Dementia. 2025.
[12] Caspar S, et al. Nonpharmacological Management of BPSD. 2018.
[13] Mercier C, et al. The treatment of behavioural and psychological symptoms in dementia. 2024.
[14] Kim SK, et al. Human-specific features of the cerebellum and ZP2-regulated synapse development. Cell. 2026. (ZP2在人类小脑颗粒细胞中富集,并由脑桥苔状纤维输入诱导,参与球状突触相关蛋白和神经活动调控)
[15] Kim SK, et al. PubMed / PMC record of Human-specific features of the cerebellum and ZP2-regulated synapse development. (ZP2与人类小脑颗粒细胞和球状突触调控相关)
[16] Human Protein Atlas. Brain tissue expression of ZP2. (ZP2在脑内的突出信号与小脑突触相关,而海马形成区总体表达极低)
[17] Cerejeira J, Lagarto L, Mukaetova-Ladinska EB. Behavioral and Psychological Symptoms of Dementia. Front Neurol. 2012. (BPSD的症状谱、患病负担及临床意义)
[18] Ahmadian N, et al. The Cerebellar Cognitive Affective Syndrome: A Meta-analysis. 2019. (小脑损害与认知、情感异常之间的稳定关联)
[19]Schmahmann JD, Sherman JC. The cerebellar cognitive affective syndrome. Brain. 1998. (最早系统提出CCAS概念)
[20]The Cerebellar Cognitive Affective Syndrome and related overview chapters. (支持小脑在执行、语言、视觉空间与情感失调中的作用)

