J Nanobiotechnol:肠道里的“特种兵”!一种益生菌能精准打击结直肠癌

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效

如今,
结直肠癌
已成为全球第二大致命癌症,每年导致近百万人死亡。在中国,随着生活方式西化和老龄化加速,结直肠癌发病率和死亡率持续攀升,且呈现年轻化趋势,更令人忧心的是,近半数患者确诊时已处于中晚期。虽然
免疫
疗法为部分患者带来希望,但绝大多数结直肠癌属于“冷肿瘤”,对PD1抑制剂等免疫检查点抑制剂反应欠佳。在这一严峻背景下,科学家们将目光投向了人体肠道内数以万亿计的微生物,其是否藏着一把对抗癌症的“钥匙”?

从益生菌到抗癌“快递员”:一场精密的分子战争
日前,一篇发表在国际杂志
Journal of Nanobiotechnology
上题为
“Bifidobacterium breve inhibits colorectal cancer via extracellular vesicles containing formate acetyltransferase”
的研究报告中,来自中山大学药学院(深圳)等机构的科学家们通过研究发现,名为短双歧杆菌的益生菌或并非通过细菌本身,而是通过其分泌的“纳米快递小车”—细胞外囊泡来执行
精准
抗癌任务;相关研究结果首次揭示了短双歧杆菌来源的囊泡及其携带的关键蛋白质如何重塑肿瘤微环境、激活免疫系统并直接杀死
癌细胞
。
该研究中的实验对象包括短双歧杆菌、小鼠结直肠癌细胞系MC38和CT26、人正常结肠上皮细胞NCM460,以及免疫功能正常和T细胞缺陷的小鼠模型。研究人员首先通过超速离心从细菌培养液中分离出细胞外囊泡,并用电镜、动态光散射等技术确认其形态完整、大小均一,平均直径约100纳米。他们还将囊泡标记上荧光染料,追踪其在体内的分布—结果令人振奋:
静脉注射
的囊泡会特异性地富集在肿瘤组织,而非肝脏、脾脏等正常器官。
实验流程层层递进,研究人员首先证实,给荷瘤小鼠口服活的双歧杆菌能显著抑制肿瘤生长,但将细菌加热灭活后,这一效果便消失殆尽。更关键的是,如果先用GW4869(一种抑制囊泡生成的化合物)处理细菌,再将其培养上清液喂给小鼠,抗癌效果同样消失,这或许表明,真正起作用的不是细菌本身而是其分泌的囊泡。
接下来,研究人员将纯化的短双歧杆菌囊泡通过尾静脉注射到荷瘤小鼠体内。结果显示,囊泡治疗组肿瘤体积和重量显著下降,肿瘤组织中杀伤性T细胞(CD8+ T细胞)的比例和活性大幅提升,其分泌的颗粒酶B、
穿孔
素和干扰素-γ水平明显升高。体外实验进一步证实,囊泡能被癌细胞高效内吞,并直接诱导癌细胞凋亡,但对正常结肠上皮细胞无毒性作用。有趣的是,在T细胞缺陷的小鼠中,囊泡的抗癌效果完全消失,说明其作用高度依赖适应性免疫系统。
囊泡治疗还重塑了荷瘤小鼠的肠道菌群,16S rRNA测序显示,治疗后小鼠肠道中双歧杆菌和乳杆菌等有益菌丰度增加,而肠道菌群Alistipes等与不良预后相关的菌属减少。功能预测分析表明,囊泡处理降低了与氨基酸代谢和能量代谢相关的通路,这些代谢途径恰好是癌细胞生长所依赖的。
那么,囊泡里到底装着什么“秘密武器”?研究者对囊泡内容物进行了质谱分析,结果发现一种名为甲酸乙酰转移酶的蛋白质高度富集,这个听起来陌生的蛋白质其实是细菌代谢中的关键酶。研究者通过基因工程在大肠杆菌中表达并纯化了这种蛋白质,然后将其直接注射到荷瘤小鼠体内。结果令人惊叹:纯化的蛋白质几乎完全复现了囊泡的抗癌效果—抑制肿瘤生长、激活杀伤性T细胞、诱导癌细胞凋亡。RNA测序揭示,这种蛋白质处理后的肿瘤组织中,颗粒酶家族成员和穿孔素表达显著上调,线粒体凋亡通路被激活,表现为促凋亡蛋白BAX、BID、APAF1增加,抗凋亡蛋白Bcl-2下降。
最后,研究者将这种蛋白质与PD1抗体联合使用,在两种结直肠癌小鼠模型中,联合治疗组的效果均优于任一单药治疗组,肿瘤内杀伤性T细胞和自然杀伤细胞的比例进一步增加,这意味着,这种细菌来源的蛋白质能够将原本对免疫治疗不敏感的“冷肿瘤”转化为“热肿瘤”从而增强PD1抗体的疗效。
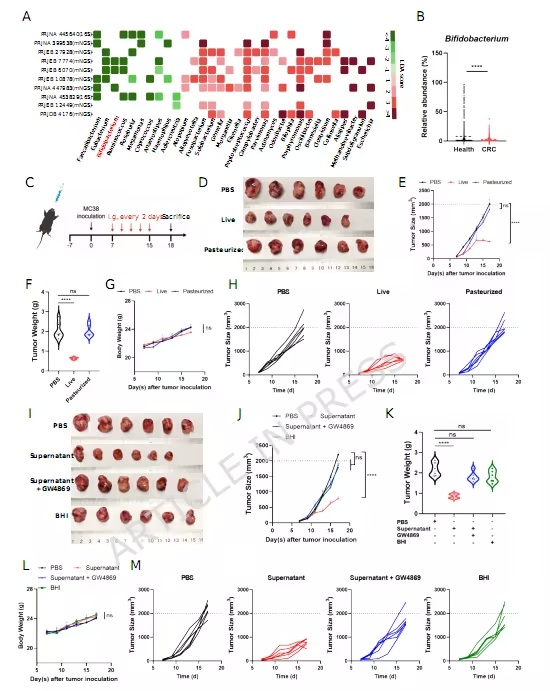
短双歧杆菌及其无细胞上清液会抑制肿瘤生长
“益生菌-囊泡-蛋白质”三级火箭:抗癌治疗的新范式
研究者表示,短双歧杆菌通过分泌携带甲酸乙酰转移酶的细胞外囊泡,以“三级火箭”的方式精准打击结直肠癌—囊泡作为纳米级快递车,将活性蛋白质安全送达战场;蛋白质激活杀伤性T细胞和自然杀伤细胞,将免疫系统从“旁观者”变为“主力军”。同时直接诱导线粒体凋亡通路,从内部瓦解癌细胞,更精妙的是,这一机制与现有免疫疗法形成协同效应,有望突破PD1抗体的耐药困境。
这项研究解释了为何益生菌抗癌的研究结果常不一致—关键在于是否产生足量活性囊泡,同时,研究人员还提出了一种“无生命”干预策略,即直接使用纯化的囊泡或活性蛋白可规避活菌制剂在免疫低下患者中可能引发的菌血症风险,他们还鉴定出一个全新的抗癌效应蛋白,为开发新型生物制剂提供了候选分子。
当然,从实验室到临床还有很长的路,这种蛋白质如何进入癌细胞、如何被免疫细胞识别、是否在人体内同样有效,仍有待验证。但至少,这项研究让我们看到,对抗结直肠癌这场艰难的战役中,答案或许就藏在每个人肠道里那些默默无闻的“微生物居民”中。(
生物谷
Bioon.com)
参考文献:
Zhang, Y., Zhang, Q., Luo, Y. et al.
Bifidobacterium breve inhibits colorectal cancer via extracellular vesicles containing formate acetyltransferase
. J Nanobiotechnol (2026). doi:10.1186/s12951-026-04275-8.

