Science:新研究揭示DNA-蛋白质交联物加速衰老

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效
尽管DNA在细胞核内被紧密包装和保护,但它不断受到来自正常代谢过程或辐射、化学物质等外部应激源的损伤威胁。为了应对这种情况,细胞依赖于一个复杂的修复机制网络。当这些系统失效时,DNA损伤会累积,损害细胞功能,并导致癌症、
衰老
和退行性疾病。

一种特别严重的DNA损伤形式是所谓的DNA-蛋白质交联物(DNA–protein crosslinks, DPCs),即蛋白质附着在DNA上。DPCs可能由饮酒、接触甲醛或其他醛类物质,或由参与DNA复制和修复的酶发生错误而引起。由于DPCs在细胞分裂过程中会阻碍DNA复制,从而可能导致严重错误,因此DNA-蛋白质交联物对基因组完整性构成严重威胁。
酶SPRTN通过切割DNA-蛋白质交联物来移除DPCs。SPRTN
功能障碍
,例如因突变所致,可能使个体在青少年时期易患骨骼
畸形
和
肝癌
。这种罕见的遗传性疾病被称为Ruijs-Aalfs综合征。其潜在机制仍知之甚少,且没有特异性疗法。
泄漏的DNA引发
免疫
警报
现在,由法兰克福歌德大学生物化学II研究所的Ivan Ðikić教授领导的研究团队证明,功能性SPRTN酶的缺失不仅导致细胞核内受损DNA的积累。通过细胞培养实验和基因修饰小鼠,他们发现,此外,来自细胞核的DNA还会泄漏到细胞内部(即细胞质)中。该研究发表在《科学》期刊上。
细胞质中的DNA被细胞识别为危险信号,因为这种DNA通常来自入侵的病毒或细菌,或来自恶性转化。因此,细胞质DNA通过启动所谓的cGAS-STING信号通路来激活防御机制。此外,细胞会释放吸引免疫细胞的信使物质,导致慢性炎症。
慢性炎症与衰老效应
这个由法兰克福领导的研究团队观察到,这种慢性炎症反应在小鼠胚胎中尤为明显,并在成年后持续存在,特别是在肺和肝脏中。结果,小鼠过早死亡或表现出与Ruijs-Aalfs综合征患者相似的早衰迹象。阻断相关的免疫反应缓解了许多症状。
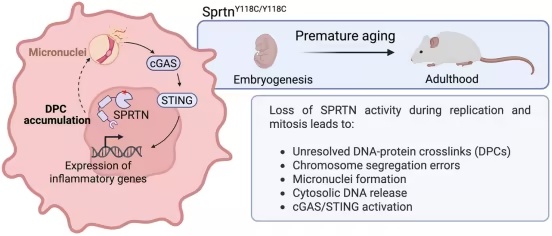
"未修复的DPCs具有更广泛的系统性后果,"Ðikić解释道。"它们不仅损害基因组稳定性,还会驱动可能显著影响寿命的慢性炎症。"
为靶向疗法打开大门
这位医生兼分子生物学家看到了开发疗法的潜力:"除了Ruijs-Aalfs综合征,还有其他罕见的遗传性疾病中DNA-蛋白质交联物起着重要作用。通过我们的工作,我们也为这些疾病未来的治疗方法奠定了重要基础。"
"通过研究这些罕见疾病的潜在机制,我们发现了DNA损伤、炎症反应和生物体寿命之间的新联系。这也增进了对衰老生物学的理解。"(
生物谷
Bioon.com)
参考文献:
Ines Tomaskovic et al,
DNA-protein cross-links promote cGAS-STING–driven premature aging and embryonic lethality
, Science (2026). DOI: 10.1126/science.adx9445.

