303个原子!全球首个蛋白质量子模拟落地

专属客服号

微信订阅号
大数据治理
全面提升数据价值
赋能业务提质增效


在量子计算的漫长青春期里,“实用化”始终是一道若隐若现的红线。
长期以来,量子计算机在生物化学领域的应用,因受限于硬件规模与算法效率,大多停留在模拟氢分子、水分或简单氨基酸的“玩具模型”阶段。然而,2026年3月,克利夫兰医学中心与IBM的一项联合研究成果,正式向科学界宣告:这条红线已被跨越。
这次突破的核心在于,研究团队在IBM Quantum Heron r2处理器上,通过全新的“以量子为中心的超级计算”(QCSC)工作流,成功模拟了包含303个原子的微型蛋白质——Trp-cage的电子结构。这不只是一个数字的跳跃,它意味着量子算力终于开始能够“切碎”具有真实工业价值的生命科学难题。正如克利夫兰医学中心Merz实验室负责人Kenneth Merz博士所言,科学界不再仅仅是在验证量子计算“能不能行”,而是在实测它“能跑多远”。这一成就标志着生物计算正式进入了“Heron时代”,量子计算开始从实验室景观走向真正的工业生产现场。

从“实验室景观”走向“工业现场”
在过去十年里,量子化学模拟的进展更像是一场关于“可能性”的展览。科学家们在几位数的量子比特上小心翼翼地复现着经典计算机早已烂熟于心的简单分子结构。虽然这证明了量子力学模拟量子系统的天然优势,但在制药巨头和材料科学家的眼中,这些“微缩景观”距离动辄成千上万原子的蛋白质结构、药物分子相互作用依然遥不可及。
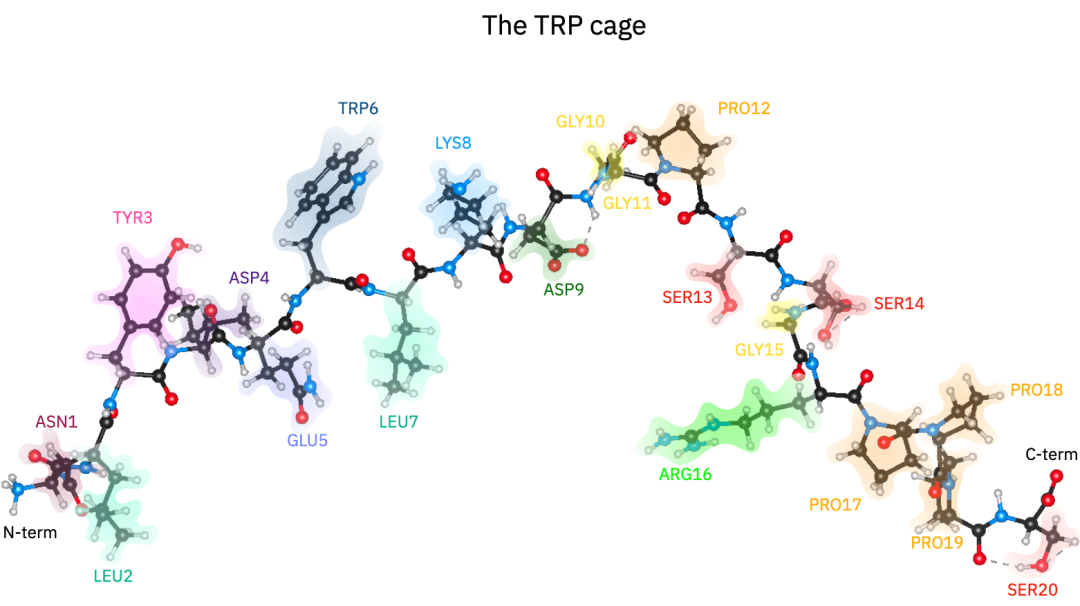
然而,Trp-cage的出现改变了这一切。虽然被称为“微型蛋白质”,但Trp-cage(色氨酸笼)拥有完整的折叠特征、疏水核心以及复杂的氢键网络。模拟它的电子结构,意味着算力必须能够精确捕捉数百个原子之间错综复杂的电子相互作用。
“我甚至要掐一下自己才能相信我们做到了,”克利夫兰医学中心Merz实验室负责人Kenneth Merz博士感慨道。这种感叹背后,是计算范式的根本性转变:我们不再仅仅是在验证量子计算“能不能行”,而是在实测它“能跑多远”。

为什么是Trp-cage?
在生物学中,理解蛋白质如何折叠、如何与水分子相互作用,是理解生命活动最底层的“说明书”。Trp-cage(色氨酸笼)虽然被称为“微型蛋白质”,但在生物物理学中是一个极具代表性的范例。它仅由20个氨基酸组成,却拥有完整的折叠特征、疏水核心以及复杂的氢键网络。模拟它的电子结构,要求算力必须能够精确捕捉数百个原子之间错综复杂的电子相互作用。
过去,这种规模的模拟在经典计算机上几乎是不可能完成的任务,因为电子组态的数量会随着分子规模呈几何级数增长。如果使用传统方法对一个包含100个氨基酸的小型蛋白质进行穷举搜索,经典计算机可能需要耗费相当于宇宙年龄的时间。而Trp-cage的成功模拟,证明了量子计算在处理复杂非共价相互作用(如氢键和疏水力)方面的独特优势。它像是一盏“标准烛光”,照亮了通往更大型、更复杂生物分子模拟的道路。研究团队已经明确表示,他们接下来的目标是瞄准膜蛋白等更具挑战性的领域。

QCSC策略之变:“化整为零”
此次模拟成功的“秘诀”并非单纯依靠堆砌量子比特,而在于一种名为“以量子为中心的超级计算”(QCSC)的新型实战策略。面对303个原子的庞然大物,目前的量子硬件尚无法通过单一算法实现全系统的整体模拟。

QCSC的逻辑极具工程美学。它不再试图让量子计算机替代经典计算机,而是将其定位为经典超算的“最强插件”。IBM在2026年3月发布的行业首个“量子中心超级计算参考架构”为此提供了技术蓝图。该架构将计算任务分为四个层级,从底层的Heron QPU硬件到顶层的应用求解器,实现了量子与经典资源的高效协同。
在这种模式下,研究团队采用了“化整为零”的波函数嵌入技术(EWF)。他们将复杂的蛋白质系统拆解成一个个“计算簇”:对于处于蛋白质边缘、电子环境相对简单的区域,利用经典超算进行处理;而对于处于分子核心、纠缠极其复杂的部分,则交给量子芯片处理。这种“按需分配”的智慧,使得量子线路能够作为节点嵌入到经典子程序中,极大地提高了计算效率。正如RIKEN研究所与IBM的协作所示,他们甚至将Heron处理器与Fugaku超算的15万个经典节点相连,成功模拟了极复杂的铁硫簇结构。
这种“化整为零、按需分配”的策略,是目前量子计算通往实用化的唯一捷径。它证明了量子计算不需要替代经典计算,而是作为经典超算的“最强插件”,去解决那些最硬的骨头。

Heron r2处理器的高光时刻
所有的算法理想都必须建立在硬件的稳定性之上。本次模拟任务运行在IBM Quantum Heron r2处理器上。
这款拥有156个量子比特的处理器,是IBM完成其2022年提出的“100x100挑战”的重要里程碑。

相较于两年前,Heron r2的表现堪称质变。它引入了两级系统(TLS)缓解技术,显著改善了全芯片的相干性,并利用先进的物理布局减少了比特间的串扰。最令人振奋的数据是它的运行速度:复杂的计算任务从以往的120小时缩短到了2.4小时,实现了近50倍的提速。这意味着,原本需要五天才能拿到的实验结果,现在一个午休的时间就能产出。
此外,Heron r2不仅在数量上超过了此前的Heron r1(133比特),在质量上也达到了新的高度。其两比特门错误率降至0.3%左右,支持高达5000次门操作,这使得它能够支撑起QCSC这种需要频繁交互、大规模迭代的混合工作流。这种“高精度生产力”的出现,标志着量子硬件已经从单纯的实验装置演进为可以支撑工业级负载的计算平台。

重塑万亿美金新药研发
传统的药物研发被业内称为“昂贵的盲选”:开发一种新药平均需要耗费10年时间和超过10亿美金,而成功率仅为10%。量子模拟的介入,正在彻底改变这一被称为“埃隆定律”的研发魔咒。
Kenneth Merz博士为我们描绘了一个极具爆发力的三步走蓝图:首先,通过QCSC工作流积累海量高精度的分子行为数据。这些由量子算力生成的模拟数据,在物理真实性上远超目前的实验观测。其次,将这些精准数据喂给AI进行训练。相比于在嘈杂、有限的实验数据上学习,AI在量子模拟数据上的预测精度将产生质的飞跃。最后,科学家向AI下达指令,AI直接设计出优化分子,最后只需在实验室进行针对性合成验证。

目前,这一愿景已经有了初步的实践。Moderna正与IBM合作,利用量子算法预测mRNA分子的折叠结构,这是设计mRNA疫苗最关键的步骤。St. Jude儿童研究医院则成功针对被认为“不可成药”的KRAS突变基因,通过量子与机器学习的结合生成了新型候选药物 。麦肯锡估算,到2035年,量子计算可为生命科学行业创造高达5000亿美元的价值。

个性化医疗与基因组学的未来
量子算力的影响并未止步于药物设计,它正深入到医疗健康的每一个细胞。在个性化医疗领域,处理海量、多维的基因组数据一直是经典计算的瓶颈。

二十五年前,人类基因组计划耗时13年才完成。而在量子时代,Wellcome Sanger研究所与Quantinuum的合作显示,量子系统能以指数级的速度处理复杂的基因组序列。这意味着未来医生可以根据每个病人的遗传特征、生活方式甚至实时变化的代谢组数据,量身定制癌症治疗方案。
在医学影像领域,量子增强的机器学习模型能够以更快的速度识别出放射图像中微小的病变迹象,比经典模型更早地预警阿尔茨海默病或癌症。甚至在放射治疗中,量子计算也能将剂量分布的计算精度提高25%,确保在杀死肿瘤的同时,最大限度减少对健康组织的伤害。

通往2029的数字化主权
模拟Trp-cage只是一个哨音。它宣告了一个时代的结束,那个计算力限制人类对生命理解的时代;同时也开启了一个新的时代,算力成为理解生命本源最强显微镜的时代。
IBM的路线图显示,他们计划在2029年交付首个大型容错量子计算机“Starling”,其操作能力预计比现在的系统提高2万倍。随着“Nighthawk”和“Cockatoo”等后续处理器的迭代,量子计算将逐步从单一的算力加速器演进为与经典超算完全融合、共同设计的统一平台。
未来的顶级药企,本质上将是一家拥有量子算力底座的计算公司。谁能掌握QCSC工作流,谁能率先积累高精度的量子模拟数据库,谁就将在未来的生物主权竞争中掌握话语权。正如这次303个原子的稳定模拟所揭示的那样:未来已在当下发生。当经典超算的边界被量子“切口”划开,一个由量子力学定义的科学新纪元正加速到来。
模拟蛋白质电子结构不仅仅是为了好玩,它是人类对生命本质的一次数字化重构。在这场竞赛中,我们不仅在挑战算力的极限,更是在重新定义人类治疗疾病和延长寿命的可能性。
[1]https://www.ibm.com/quantum/blog/cleveland-clinic-protein-qcsc
[2]https://research.ibm.com/publications/quantum-hfdft-embedding-algorithms-for-electronic-structure-calculations-scaling-up-to-complex-molecular-systems
[3]https://pubs.acs.org/doi/10.1021/bi501021r
[4]https://postquantum.com/industry-news/ibm-heron-r2-quantum/







